Серная кислота аккумуляторная
Описание:Серная кислота — бесцветная маслянистая жидкость, не имеющая запаха. С водой и серным ангидридом смешивается в любых соотношениях с выделением большого количества тепла. Контактная серная кислота с массовой долей моногидрата 92,5-94,0% является водным раствором моногидрата (100% серной кислоты). В технике под серной кислотой подразумевают любые соединения H2SO4 с водой. Водные растворы серной кислоты характеризуются массовой долей в них H2SO4 или SO3
Серная кислота — одна из самых активных неорганических кислот. Она реагирует почти со всеми металлами и их оксидами, вступает в реакции обмена, обладает окислительными и другими важными свойствами. Основные физико-химические свойства растворов серной кислоты зависят от соотношения в ней воды и серного ангидрида (триоксида серы).
Применение:Серная кислота используется в производстве минеральных удобрений, красителей, химических волокон, а также в металлургии.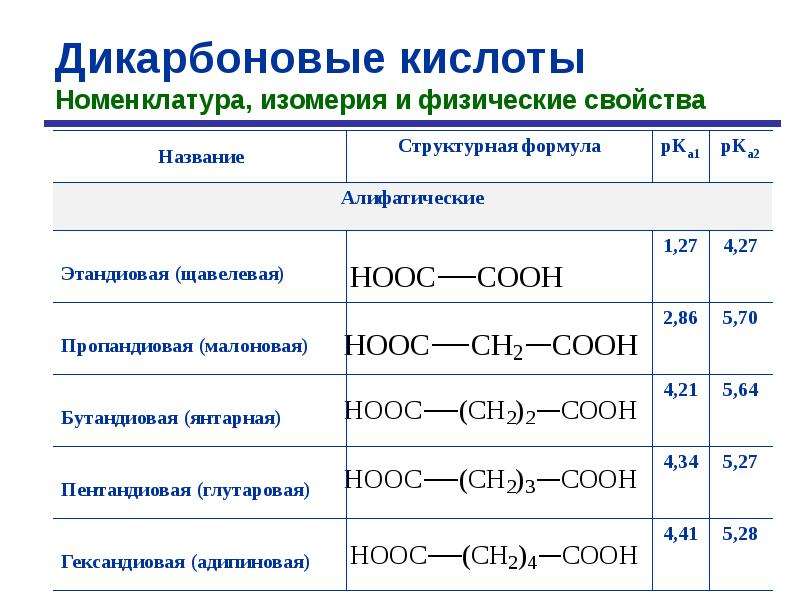
В качестве электролита для аккумуляторных батарей применяют раствор серной аккумуляторной кислоты в дистиллированной воде. Для различных климатических и температурных условий, в которых батарее предстоит работать, используют электролит различной плотности. Плотность электролита зависит от концентрации раствора серной аккумуляторной кислоты — чем больше концентрация раствора, тем больше плотность электролита и от температуры раствора — чем выше температура, тем ниже плотность. Концентрация или плотность электролита является точным критерием степени разряженности аккумулятора. В качестве точки отсчета, для определения текущей степени разряженности аккумулятора, принимается нормативная плотность электролита, т.е. плотность, приобретенная после первого полого заряда.
Серная кислота
ГОСТ 667-73
Влияние суперпластификатора и ускорителя набора прочности ПФМ-НЛК на подвижность бетонной смеси и прочностные характеристики бетона
| Технические характеристики | Высший сорт | Первый сорт |
|---|---|---|
| Массовая доля моногидрата (H2SO |
92-94 | 92-94 |
| Массовая доля железа (Fe), % | 0,005 | 0,01 |
| Массовая доля остатка после прокаливания, %, не более | 0,02 | 0,03 |
| Массовая доля оксидов азота (N2O4), %, не более | 0,00003 | 0,00001 |
| Массовая доля мышьяка (As), %, не более | 0,00005 | 0,00008 |
| Массовая доля хлористых соединений (Cl), %, не более | 0,0002 | 0,0003 |
| Массовая доля марганца (Mn), %, не более | 0,00005 | 0,0001 |
| Массовая доля суммы тяжелых металлов в пересчете на свинец (Pb), %, не более | 0,01 | 0,01 |
| Массовая доля меди (Cu), %, не более | 0,0005 | 0,0005 |
| Массовая доля веществ, восстанавливающих KMnO4, см3 раствора с (1/5 KMnO4 |
4,5 | 7 |
| Прозрачность | Должна выдерживать испытание по п. 3.13 3.13 |
|
Серная кислота упаковывается в ж/д и авто цистерны, канистры, кубовые емкости.
Хранение:Техническая серная кислота и олеум (концентрированная серная кислота) должны храниться в емкостях из стали или спецстали, как нефутерованных, так и футерованных кислотоупорным кирпичом или кислотоустойчивым материалом.
Транспортировка:
Серную кислоту техническую транспортируют в железнодорожных сернокислотных цистернах в соответствии с правилами перевозок грузов. На цистерны должны быть нанесены специальные трафареты в соответствии с правилами перевозок грузов, действующими на ж.д. транспорте. Техника безопасности:
Кислота серная пожаро- и взрывобезопасна, при соприкосновении ее с водой происходит бурная реакция с большим выделением тепла, паров и газов. Токсична. По степени воздействия на организм относится к веществам 2-го класса опасности.
 При работе с серной кислотой обязательно применять спецодежду.
При работе с серной кислотой обязательно применять спецодежду.Аккумуляторная кислота формула
Какая кислота в аккумуляторе автомобиля
Практически все владельцы личного транспортного средства прекрасно знают о том, что в аккумуляторах есть кислота. Даже новички, которые только начинают постигать азы вождения, и то осведомлены касательно этого вопроса.
Многие из них слышали о кислотно-свинцовых аккумуляторах, но на деле так и не имеют представления, как именно работает это устройство. А между тем здесь протекают определенные химические реакции.
Какая кислота в аккумуляторе и для чего нужна
Большинство автомобилистов прекрасно знают, какая кислота залита в аккумуляторе. Но находятся и те, кто считают, что внутри аккумулятора ничего кроме дистиллированной воды (или дистиллята) нет. Другие же придерживаются мнения в пользу соляной кислоты, которое также неверно.
В любой автомобильной батарее содержится серная кислота — H2SO4. Если быть точнее, то речь идет о растворе серной кислоты с дистиллированной водой. Такая жидкость имеет общее название – электролит. Так какова роль серной кислоты?
Если быть точнее, то речь идет о растворе серной кислоты с дистиллированной водой. Такая жидкость имеет общее название – электролит. Так какова роль серной кислоты?
Это основной компонент для работы АКБ. В отсутствие кислоты невозможен процесс заряда и разряда батареи. Это одна из самых активных разновидностей, которая способна вступать во взаимодействие практически с любым металлом, включая их оксиды. К тому же кислота может вступать в реакции обмена, а ее активность зависит от содержания воды.
Когда происходит заряд кислотного аккумулятора, пластины из чистого свинца (отрицательные) начинаются выделять электроны, которые принимаются решетками из оксида свинца (положительные). При разряде батареи происходит в точности до наоборот. Иными словами, когда пластины отдают электроны, они как бы «разрушаются» – происходит заряд, а при разряде они возвращаются обратно, что именуется «восстановлением».
И вот как раз для такого процесса разрушения – восстановления и нужна агрессивная среда в виде разбавленной серной кислоты. И без нее эффективность автомобильных батарей была бы на очень низком уровне.
И без нее эффективность автомобильных батарей была бы на очень низком уровне.
Состав электролита и как правильно сделать
Серная кислота широко используется в современной промышленности для получения электрической энергии (аккумуляторы, батареи, электрические конденсаторы). Что касается состава электролита в АКБ, то соотношение между серной кислотой и дистиллированной водой следующее:
- сама кислота – 30%;
- дистиллированная вода – 70%.
Именно такая субстанция эффективным образом взаимодействует со свинцовыми пластинами. При этом особого внимания заслуживает плотность электролита, на что непосредственным образом оказывает влияние серная кислота. У концентрированной она достигает показателя в 1,83 г/см3. Добавлением дистиллированной воды обеспечивается понижение плотности до нужных пределов – обычно это диапазон 1,23-1,27 г/см3.
| Плотность электролита (г/см3) | Напряжение без нагрузки (В) | Напряжение с нагрузкой (В) | Степень заряженности (%) | Замерзание электролита (С) |
|---|---|---|---|---|
| 1,27 | 12,66 | 10,8 | 100 | -60 |
| 1,26 | 12,6 | 10,66 | 94 | -55 |
| 1,25 | 12,54 | 10,5 | 87,5 | -50 |
| 1,24 | 12,48 | 10,34 | 81 | -46 |
| 1,23 | 12,42 | 10,2 | 75 | -42 |
| 1,22 | 12,36 | 10,06 | 69 | -37 |
| 1,21 | 12,3 | 9,9 | 62,5 | -32 |
| 1,2 | 12,24 | 9,74 | 56 | -27 |
| 1,19 | 12,18 | 9,6 | 50 | -24 |
| 1,18 | 12,12 | 9,46 | 44 | -18 |
| 1,17 | 12,06 | 9,3 | 37,5 | -16 |
| 1,16 | 12 | 9,14 | 31 | -14 |
| 1,15 | 11,94 | 9 | 25 | -13 |
| 1,14 | 11,88 | 8,84 | 19 | -11 |
| 1,13 | 11,82 | 8,68 | 12,56 | -9 |
| 1,12 | 11,76 | 8,54 | 6 | -8 |
| 1,11 | 11,7 | 8,4 | 0,0 | -7 |
Знать этот параметр необходимо для понимания порога замерзания электролита.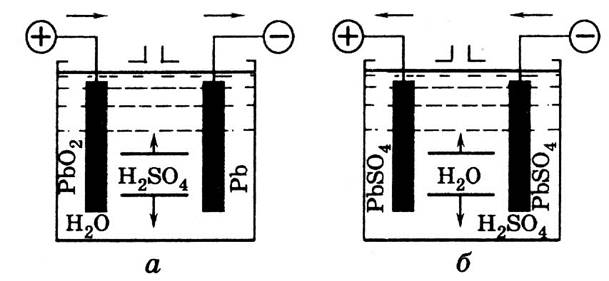 При плотности в 1,11 г/см3 субстанция замерзает уже под воздействием относительно небольшого холод: -7 °C. У рекомендованных значений порог этот существенно отличен – от -58 °C до -64 °C. А можно ли самому сделать электролит?
При плотности в 1,11 г/см3 субстанция замерзает уже под воздействием относительно небольшого холод: -7 °C. У рекомендованных значений порог этот существенно отличен – от -58 °C до -64 °C. А можно ли самому сделать электролит?
Да, это действительно возможно, только действовать необходимо с предельной осторожностью. И поскольку предстоит иметь дело с серной кислотой высокой концентрации, то такая работа представляет определенную опасность. Необходимо позаботиться о защите рук, тела, органов дыхания.
Собственно в том, чтобы самостоятельно приготовить электролит для АКБ, нет ничего сложного – смешать серную кислоту с дистиллированной водой, соблюдая пропорцию. Стоит заметить, что обычна вода из-под крана для таких целей не подходит, поскольку содержит большое количество разных примесей, которые негативным образом воздействуют на свинцовые пластины.
Собственно сами ингредиенты:
- Серная кислота (плотность должна быть 1,83 г/см3 или более, но не менее).

- Дистиллированная вода.
- Любая фарфоровая посуда.
Пропорции кислоты и воды нам известны – 30% и 70% соответственно. При этом важен характер подхода к производству – оптимально кислоту добавлять в воду, а не наоборот. Также стоит учесть, что при их смешивании будет выделяться очень много тепловой энергии и по этой причине недопустимо использовать стеклянную посуду – она просто лопается. Когда температура электролита упадет, его можно перелить в стеклянную емкость или тару из пластика.
После того как жидкости будут соединены, следует замерить плотность ареометром. Если показатели соответствуют допустимому пределу, электролит готов к эксплуатации. Но такое приспособление имеется далеко не у каждого водителя, а поэтому пригодится следующая подсказка плотности электролита (из расчета на 1 литр дистиллированной воды):
- при 1,23г/см3 – 280г;
- при 1,25г/см3 – 310г;
- при 1,27г/см3 – 345 г;
- при 1,29г/см3 – 385 г.

Собственно на этом работа и заканчивается. Тем, кто проживает в средней полосе России, следует придерживаться плотности – 1,27 г/см3. При этом для зон с холодным климатом (до -30 °С) допустимый показатель составляет 1,26-1,28 г/см3, а жарких субтропических районов – 1,24-1,26 г/см3. Пределы плотности от 1,27 г/см3 до 1,29 г/см3 актуальны для тех регионов, где зима свирепствует до -50 °С.
К чему приведет нарушение рецептуры
Показатель в 1,29 г/см3 является не самым высоким – встречается концентрат электролита с плотностью 1,33 г/см3 (применяется для корректировки), ранее можно было найти даже с плотность 1,4 г/см3, но сейчас он снят с продажи. Однако его все же следует также разбавить водой и только после этого заливать внутрь АКБ. Почему же нельзя лить сильно концентрированный электролит?
Ничего хорошо уж точно не произойдет! Из-за высокой концентрации страдают пластины аккумулятора – их просто разъедает со временем. Это происходит медленно, но верно! Поэтому, если залить высокий концентрат, не следует удивляться тому, что АКБ в скором времени вышла из строя.
Это происходит медленно, но верно! Поэтому, если залить высокий концентрат, не следует удивляться тому, что АКБ в скором времени вышла из строя.
Низкая плотность электролита приводит к такому явлению, которое называется сульфатацией. Об этом процессе известно многим опытным водителям. В результате на пластинах оседают кристаллы сульфита свинца, из-за чего металл утрачивает способность к накоплению заряда.
К тому же, как выше уже было упомянуто, из-за слишком низких показателей плотности электролит замерзает, обращаясь в лед. Чем это грозит, каждому уже понятно – повреждения пластин не избежать.
Как корректировать плотность жидкости
Владельцам автомобилей необходимо контролировать уровень электролита и его плотность. Из-за гидролиза и нагрева АКБ в подкапотном пространстве содержание субстанции понижается, а плотность наоборот растет. По этой причине возникает необходимость доливать дистиллированную воду. Но иногда показатели плотности электролита могут стать меньше нормы. Тогда следует поднять концентрацию кислоты.
Тогда следует поднять концентрацию кислоты.
Существуют несколько способов как это можно сделать, исходя из степени понижения плотности электролита. Для этого следует замерить его концентрацию в каждой банке по отдельности. Если густота электролита получена от 1,18 г/см3 до 1,20 г/см3, то оптимальное решение – замена части электролита в банке на новый с плотностью 1,27 г/см3. Иными словами делается повышение плотности электролита.
Только предварительно стоит убедиться в том, что АКБ заряжена, иначе батарею следует подзарядить. При низком заряде аккумулятора к такой процедуре нельзя приступать. Иначе концентрация H2SO4 резко поднимется, что приведет только к разрушению пластин.
Сама же процедура выполняется в следующем порядке:
- Резиновой грушей откачивает как можно больше жидкости из банки. При этом замерить объем.
- Добавляют новый корректирующую жидкость с плотностью 1,27-1,29 гр/см3 в количестве равном половине изъятого объема.

- Пусть все перемешается между собой – для этого можно дать нагрузку на выводы, просто подождать некоторое время или потрясти АКБ.
- Замеряют плотность. Если показатели по-прежнему не достигли допустимых пределов доливку электролита стоит продолжать до достижения нужных параметров.
- Когда предел установлен, банки закрывают, а сам аккумулятор ставится на зарядку.
В том случае, когда плотность электролита снижена ниже уровня в 1,2 гр/см3, тогда необходимо менять его полностью – сливать старый, заливать новый.
Электролит: основа свинцово-кислотных автомобильных аккумуляторов
В качестве стартерных батарей в автотранспорте используются свинцово-кислотные аккумуляторы. Функционирование аккумулятора обеспечивается специальным раствором серной кислоты — электролитом. О том, что такое аккумуляторный электролит, каких типов он бывает, и как его использовать — читайте в статье.
Что такое электролит?
Аккумуляторный электролит — водный раствор серной кислоты, предназначенный для использования в свинцово-кислотных аккумуляторных батареях (АКБ). Электролит готовится путем растворения концентрированной серной кислоты в дистиллированной воде, молекулы кислоты в данном растворе диссоциируют (распадаются) на ионы — это явление наделяет электролит электропроводящими свойствами.
Электролит готовится путем растворения концентрированной серной кислоты в дистиллированной воде, молекулы кислоты в данном растворе диссоциируют (распадаются) на ионы — это явление наделяет электролит электропроводящими свойствами.
Аккумуляторный электролит имеет следующее назначение:
- Изготовление аккумуляторных батарей;
- Ввод в эксплуатацию сухозаряженных батарей;
- Восстановление АКБ при загрязнении или утечке электролита, коротких замыканиях между пластинами и других неисправностях.
Но прежде, чем применять электролит для той или иной цели, необходимо разобраться в его характеристиках и особенностях применения.
Зачем в аккумуляторе электролит?
Электролит, свинцовые пластины и пористый диоксид свинца (PbO2) — три основных компонента свинцово-кислотного аккумулятора. Именно в присутствии кислотного электролита протекают электрохимические реакции, делающие возможным накопление и отдачу аккумулятором электрического заряда.
Во время разряда АКБ металлический свинец и оксид свинца вступают в реакцию с серной кислотой (точнее — с ее отрицательными ионами SO4 и положительными ионами H), образуя сульфат свинца (PbSO4) и воду, при этом на анодных пластинах выделяются избыточные электроны. На катодных пластинах, напротив, наблюдается недостаток электронов, благодаря этому при замыкании анода и катода между ними возникает электрический ток. Во время заряда АКБ проходят обратные реакции — под действием тока от стороннего источника из сульфата свинца образуются чистый свинец, диоксид свинца и кислота.
В ходе данных реакций количество серной кислоты и воды в электролите изменяется, что приводит к изменению его плотности и объема. При разряде АКБ концентрация кислоты понижается, а концентрация воды немного увеличивается, что приводит к падению плотности и к некоторому увеличению объема электролита. В процессе заряда плотность повышается, а объем несколько понижается.
Типы и характеристики электролитов
Электролит изготавливается смешиванием концентрированной серной кислоты и дистиллированной воды в строго определенных пропорциях. Для изготовления электролита используется специальная аккумуляторная серная кислота (по ГОСТ 667-73) и дистиллированная вода (по ГОСТ 6709-72). Данный раствор используется во всех типах современных свинцово-кислотных аккумуляторов.
Для изготовления электролита используется специальная аккумуляторная серная кислота (по ГОСТ 667-73) и дистиллированная вода (по ГОСТ 6709-72). Данный раствор используется во всех типах современных свинцово-кислотных аккумуляторов.
Главная характеристика электролита — плотность. Для нормальной работы АКБ плотность электролита должна лежать в пределах 1,23-1,4 г/куб. см, так как именно при такой плотности раствор имеет максимальную электропроводность. Однако плотность концентрированной серной кислоты составляет 1,83 г/куб. см, поэтому для достижения необходимой плотности кислота смешивается с водой.
Плотность электролита в значительной степени зависит от двух параметров: температуры и степени заряда аккумулятора.
О зависимости плотности электролита в зависимости от заряда АКБ мы сказали выше: при заряде плотность повышается, при разряде — понижается. Зависимость плотности электролита от температуры простая: при снижении температуры плотность падает, при повышении — возрастает. Поэтому нормальная плотность определяет при температуре +25°C, а чтобы верно измерять плотность при любой температуре, используют таблицу поправок к показаниям ареометра:
Поэтому нормальная плотность определяет при температуре +25°C, а чтобы верно измерять плотность при любой температуре, используют таблицу поправок к показаниям ареометра:
| Температура электролита, °C |
Поправка к показаниям ареометра, г/куб. см |
|---|---|
| -55 … -41 | -0,05 |
| -40 … -26 | -0,04 |
| -25 … -11 | -0,03 |
| -10 … +4 | -0,02 |
| +5 … +19 | -0,01 |
| +20 … +30 | 0 |
| +31 … +45 | +0,01 |
| +46 … +60 | +0,02 |
Например, если электролит при температуре +25°C имеет плотность 1,28 г/куб. см, то при температуре -15°C он имеет плотность 1,25 г/куб. см, а при нагреве до +50°C (что часто бывает в подкапотном пространстве автомобиля) плотность повышается до 1,3 г/куб. см.
Чтобы компенсировать изменение плотности электролита в АКБ транспортных средств, эксплуатируемых в различных климатических поясах, применяются электролиты большей или меньшей плотности:
- Летние и для жаркого климата — плотностью 1,23-1,24 г/куб.
 см;
см; - Для умеренного и холодного климата — 1,27-1,28 г/куб.см;
- Зимние и для холодного климата — 1,3-1,34 г/куб.см.
Кроме того, при повышении плотности электролита повышается его морозоустойчивость — более плотные электролиты устойчивы к замерзанию, поэтому они лучше подходят для эксплуатации в холодное время года и в холодных климатических поясах.
Сегодня можно купить электролит необходимой плотности, освободив себя от непростой процедуры приготовления правильного по характеристикам электролита из кислоты и воды. Электролит продается в тарах емкостью от 1 до 20 литров, поэтому всегда можно приобрести нужный для работы объем.
Использование аккумуляторного электролита
Сразу нужно отметить, что электролит не используется для текущего обслуживания аккумулятора. Наиболее часто в АКБ снижается уровень электролита и падает его уровень, в этом случае обслуживание выполняется добавлением воды. Дело в том, что в процессе работы аккумулятора из электролита испаряется вода, а кислота остается на месте. Также потеря воды может возникать в случае перезаряда аккумулятора — при достижении определенной плотности концентрация серной кислоты в электролите снижается и ее уже не хватает для нормального протекания указанных выше электролитических реакций. В этих условиях начинается процесс электрохимического разложения воды на водород и кислород — это проявляется «кипением» электролита, а образовавшиеся газы улетучиваются. В обоих случаях — при испарении и разложении воды — плотность электролита повышается, для ее восстановления необходимо использовать воду.
Также потеря воды может возникать в случае перезаряда аккумулятора — при достижении определенной плотности концентрация серной кислоты в электролите снижается и ее уже не хватает для нормального протекания указанных выше электролитических реакций. В этих условиях начинается процесс электрохимического разложения воды на водород и кислород — это проявляется «кипением» электролита, а образовавшиеся газы улетучиваются. В обоих случаях — при испарении и разложении воды — плотность электролита повышается, для ее восстановления необходимо использовать воду.
Наиболее часто электролит применяется для восстановления работы аккумулятора в случае замерзания электролита с последующей потерей его характеристик. Если электролит в АКБ замерз, то, прежде всего, необходимо занести его в теплое помещение и дождаться оттаивания. После этого аккумулятор следует поставить на зарядку с малым током — рекомендуется ток около 1 ампера и срок зарядки до 2 суток. В ходе зарядки нужно измерять плотность электролита, если она начнет повышаться, то его можно нормально зарядить и эксплуатировать.
Если же ни при каких условиях плотность не повышается, то следует произвести замену электролита. Это выполняется следующим образом:
- Слить электролит из всех банок батареи;
- Промыть банки дистиллированной водой;
- Добавить новый электролит до указанного уровня;
- Оставить аккумулятор на 2-3 часа для пропитки пластин электролитов;
- Зарядить АКБ малым током 0,5-1 ампер в течение 2 суток.
Зарядку следует остановить, когда плотность электролита и напряжение на клеммах будут стабильными в течение хотя бы двух часов.
Но если замерзание аккумулятора вызвало деформацию или разрушение пластин, то менять электролит уже бесполезно — нужно покупать новую батарею.
Аналогично устраняются и другие проблемы с аккумулятором — утечка или загрязнение электролита, ремонт АКБ после короткого замыкания и т.д. Но в этих случаях прежде нужно проверить аккумулятор на целостность и ремонтопригодность, при обнаружении трещин и других физических повреждений батарея ремонту не подлежит, ее нужно утилизировать.
Особый случай — ввод в эксплуатацию сухозаряженных аккумуляторов, которые поставляются без электролита. Обычно для подготовки такого аккумулятора его нужно заполнить электролитом и дождаться достижения необходимой плотности — все эти действия обязательно прописаны в инструкции к аккумулятору. Предварительную зарядку сухозаряженного АКБ проводить не нужно!
Во всех случаях необходимо правильно рассчитывать объем электролита, чтобы сделать правильную покупку. Объем электролита в АКБ зависит от его напряжения и электрической емкости. Наиболее распространенные 12-вольтовые аккумуляторные батареи емкостью 55-60 А·ч вмещают 2,5-3 литра, емкостью 75-90 А·ч — от 3,5 до 5 литров. Большие 24-вольтовые АКБ емкостью свыше 100 А·ч могут содержать 10 и более литров электролита. При покупке рекомендуется брать электролит с небольшим запасом, так как в процессе работы возможны непредвиденные потери и утечки.
Серная кислота аккумуляторная
Описание:Серная кислота — бесцветная маслянистая жидкость, не имеющая запаха. С водой и серным ангидридом смешивается в любых соотношениях с выделением большого количества тепла. Контактная серная кислота с массовой долей моногидрата 92,5-94,0% является водным раствором моногидрата (100% серной кислоты). В технике под серной кислотой подразумевают любые соединения H2SO4 с водой. Водные растворы серной кислоты характеризуются массовой долей в них H2SO4 или SO3
С водой и серным ангидридом смешивается в любых соотношениях с выделением большого количества тепла. Контактная серная кислота с массовой долей моногидрата 92,5-94,0% является водным раствором моногидрата (100% серной кислоты). В технике под серной кислотой подразумевают любые соединения H2SO4 с водой. Водные растворы серной кислоты характеризуются массовой долей в них H2SO4 или SO3
Серная кислота — одна из самых активных неорганических кислот. Она реагирует почти со всеми металлами и их оксидами, вступает в реакции обмена, обладает окислительными и другими важными свойствами. Основные физико-химические свойства растворов серной кислоты зависят от соотношения в ней воды и серного ангидрида (триоксида серы).
Применение:Серная кислота используется в производстве минеральных удобрений, красителей, химических волокон, а также в металлургии. Она применяется для различных технологических целей в текстильной, пищевой и др.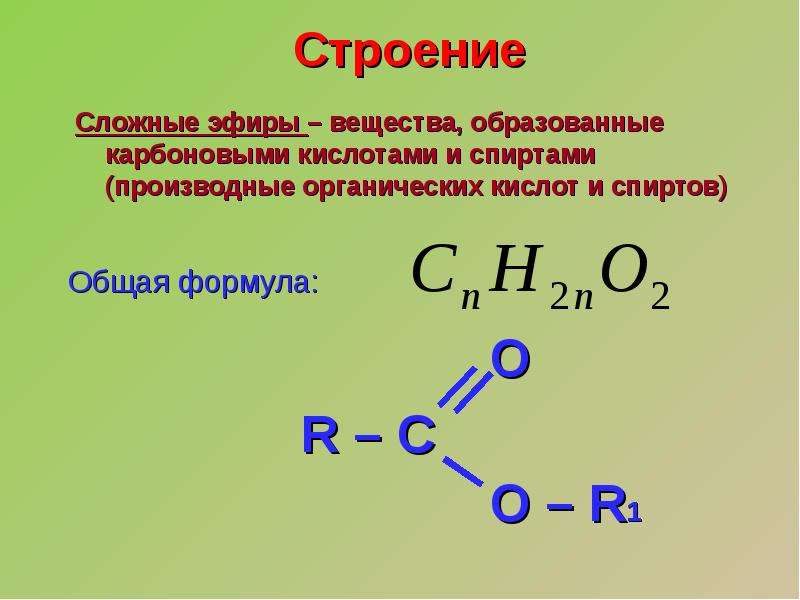 отраслях промышленности. Аккумуляторная серная кислота применяется после разбавления ее дистиллированной водой в качестве электролита для заливки свинцовых аккумуляторов.
отраслях промышленности. Аккумуляторная серная кислота применяется после разбавления ее дистиллированной водой в качестве электролита для заливки свинцовых аккумуляторов.
В качестве электролита для аккумуляторных батарей применяют раствор серной аккумуляторной кислоты в дистиллированной воде. Для различных климатических и температурных условий, в которых батарее предстоит работать, используют электролит различной плотности. Плотность электролита зависит от концентрации раствора серной аккумуляторной кислоты — чем больше концентрация раствора, тем больше плотность электролита и от температуры раствора — чем выше температура, тем ниже плотность. Концентрация или плотность электролита является точным критерием степени разряженности аккумулятора. В качестве точки отсчета, для определения текущей степени разряженности аккумулятора, принимается нормативная плотность электролита, т.е. плотность, приобретенная после первого полого заряда. Для свинцовых аккумуляторов характерно сильное разбавление электролита во время разряда из-за участия в реакции серной аккумуляторной кислоты с образованием воды. В заряженных аккумуляторах концентрация кислоты равна 30…40%. Чем меньше объем электролита, в сравнении с массой электродов, тем быстрее снижается концентрация кислоты при разряде. В конце разряда она составляет от 10 до 25%.
В заряженных аккумуляторах концентрация кислоты равна 30…40%. Чем меньше объем электролита, в сравнении с массой электродов, тем быстрее снижается концентрация кислоты при разряде. В конце разряда она составляет от 10 до 25%.
Серная кислота
ГОСТ 667-73
Влияние суперпластификатора и ускорителя набора прочности ПФМ-НЛК на подвижность бетонной смеси и прочностные характеристики бетона
| Технические характеристики | Высший сорт | Первый сорт |
|---|---|---|
| Массовая доля моногидрата (H2SO4), % | 92-94 | 92-94 |
| Массовая доля железа (Fe), % | 0,005 | 0,01 |
| Массовая доля остатка после прокаливания, %, не более | 0,02 | 0,03 |
| Массовая доля оксидов азота (N2O4), %, не более | 0,00003 | 0,00001 |
| Массовая доля мышьяка (As), %, не более | 0,00005 | 0,00008 |
| Массовая доля хлористых соединений (Cl), %, не более | 0,0002 | 0,0003 |
| Массовая доля марганца (Mn), %, не более | 0,00005 | 0,0001 |
| Массовая доля суммы тяжелых металлов в пересчете на свинец (Pb), %, не более | 0,01 | 0,01 |
| Массовая доля меди (Cu), %, не более | 0,0005 | 0,0005 |
| Массовая доля веществ, восстанавливающих KMnO4, см3 раствора с (1/5 KMnO4) = 0,01 моль/дм3, не более | 4,5 | 7 |
| Прозрачность | Должна выдерживать испытание по п. 3.13 3.13 |
|
Серная кислота упаковывается в ж/д и авто цистерны, канистры, кубовые емкости.
Хранение:Техническая серная кислота и олеум (концентрированная серная кислота) должны храниться в емкостях из стали или спецстали, как нефутерованных, так и футерованных кислотоупорным кирпичом или кислотоустойчивым материалом.
Транспортировка:
Серную кислоту техническую транспортируют в железнодорожных сернокислотных цистернах в соответствии с правилами перевозок грузов. На цистерны должны быть нанесены специальные трафареты в соответствии с правилами перевозок грузов, действующими на ж.д. транспорте.
Кислота серная пожаро- и взрывобезопасна, при соприкосновении ее с водой происходит бурная реакция с большим выделением тепла, паров и газов. Токсична. По степени воздействия на организм относится к веществам 2-го класса опасности. При работе с серной кислотой обязательно применять спецодежду.

что залито в аккумулятор, состав кислотного электролита, из чего он состоит
Автомобильные аккумуляторы извлекают электрическую энергию из химической реакции, протекающей внутри него. по сути АКБ конвертируют энергию из электрической в химическую в процессе заряда и наоборот, когда выдают необходимый ток.
Для качественного протекания этих процессов требуются ингредиенты достаточной чистоты. Особенно это касается серной кислоты, вместе с дистиллированной водой являющейся тем, из чего состоит электролит в аккумуляторе.
Серная кислота в аккумуляторе
По сути то, что залито в аккумулятор — это разбавленная серная кислота. В основе работы любого свинцово-кислотного аккумулятора лежит химический процесс, высвобождающий электрический заряд. Молекулы серной кислоты расщепляют посредством электролитической диссоциации свинцовые электроды, создавая положительно и отрицательно заряженные ионы.
Собираясь на положительных и отрицательных электродах батареи, ионы создают на клеммах АКБ необходимый заряд. Со временем часть молекул связывается без возможности возобновить свою работу в банках, что снижает плотность электролита. Поэтому так важно следить за концентрацией аккумуляторной кислоты.
Со временем часть молекул связывается без возможности возобновить свою работу в банках, что снижает плотность электролита. Поэтому так важно следить за концентрацией аккумуляторной кислоты.
Процесс носит название электролитической диссоциации. При нём ионы с положительным зарядом(катионы) — устремляются к плюсовому электроду. К отрицательному электроду направляются анионы — отрицательно заряженные ионы.
Окислителем выступает диоксид свинца, который в результате взаимодействия с молекулами кислоты восстанавливается, отдавая отрицательный заряд на электроды. Растворы серной кислоты слабо проводят электрический ток, однако хорошо справляется с ионным обменом.
При разрядке АКБ положительные ионы свинца устремляются через электролит с губчатого свинца – восстановителя. Здесь происходит превращение в двухвалентный свинец из четырехвалентного, таким образом, оставляя заряд 2 электронов с каждого иона.
На аноде — PbO2 + SO42− + 4H+ + 2e− -> PbSO4 + 2H2O — окисление свинца.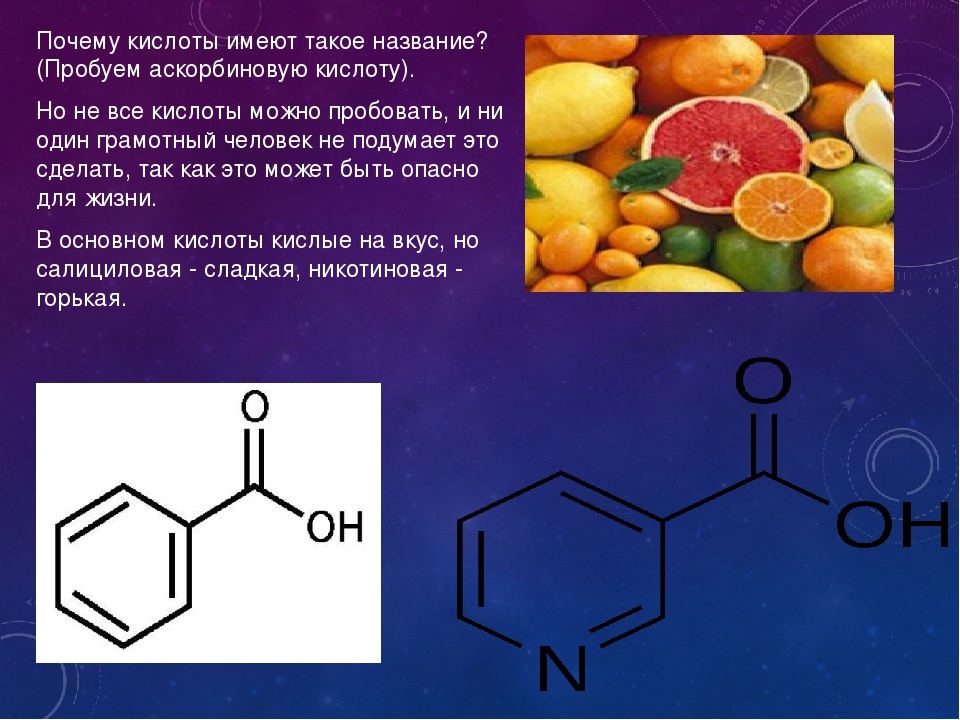
На катоде — Pb + SO42− − 2e− ->PbSO4
Во время зарядки идут обратные реакции — свинец движется в сторону пластин.
Оба электрода покрываются слоем сульфата, который образовывается из отрицательных кислотных остатков и положительных двухвалентных ионов свинца. Это называется сульфатацией, которая для пластин аккумулятора весьма опасна и грозит быстрым износом. Выделяемые газы в процессе восстановительно-окислительных реакций считаются побочным эффектом, однако они могут серьёзно повлиять на работоспособность всей батареи.
В процессе разрядки батареи к отрицательно заряженному электроду устремляются электроны, где они производят нейтрализацию ионов свинца. В зависимости от уровня заряда батареи плотность электролита может иметь разное значение.
Измерения делаются при комнатной температуре + 25 °С. Использование кислоты происходит в 1,6 раз больше положительными электродами. Поэтому рост объема электролита наблюдается при разрядке батареи и уменьшение – при зарядке.
Состав кислотного электролита
Свинцово — кислотные аккумуляторы для автомобилей наиболее распространенные на сегодня. Электролит в аккумуляторе автомобиля это 33-38 % раствор серной кислоты в дистиллированной воде. Плотность такого раствора примерно равна 1.27 г/л. Существует несколько стандартов качества кислоты, но нас интересует только характеристики кислоты для АКБ.
Согласно ГОСТ 667 73 аккумуляторная кислота должна обладать следующими физико-химическими показателями.
Для высшего сорта массовые части:
- моногидрата – 92-94 %;
- железа – до 0,005 %;
- после прокаливания остатка – 0,02 %;
- окислов азота – 0,00003 %;
- мышьяка – не более 0,00005 %;
- хлористых соединений – 0,0002 %;
- марганца – до 0,00005 %;
- всех тяжелых металлов, пересчет на Рb – 0,01 %;
- меди – 0,0005 %;
- восстановителей для KМnO – до 4,5 %.
Прозрачность раствора определяется при комнатной температуре жидкости с помощью специального теста. Согласно ГОСТ 667 73 кислота аккумуляторная должна быть определенной прозрачности, что при установке на поле с шахматными клетками и подсвечивании его электрической лампой должно давать четкие очертания ячеек. Представленные данные — это эталонные показатели, и на практике то что заливают в аккумулятор всегда ниже качеством и больше загрязнено.
Согласно ГОСТ 667 73 кислота аккумуляторная должна быть определенной прозрачности, что при установке на поле с шахматными клетками и подсвечивании его электрической лампой должно давать четкие очертания ячеек. Представленные данные — это эталонные показатели, и на практике то что заливают в аккумулятор всегда ниже качеством и больше загрязнено.
Поднятие плотности в АКБ
Повышение плотности электролита происходит как следствие повышения температуры и гидролиза в батарее. Для выравнивания этого показателя требуется постоянное добавление определенного количества дистиллята. При меньшей концентрации аккумуляторной кислоты в электролите, следует ее поднимать, если датчик показывает значение ниже 1,275 г на куб. см.
Важно! Кислота является агрессивной средой для тканей человека, одежды. Поэтому при работах с открытой батареей следует позаботиться о мерах защиты: надеть защитные очки и резиновые перчатки. Не помешает прорезиненный фартук или старая одежда.
Кислотность электролита поднимается двумя путями: внесением концентрированной кислоты с помощью постепенного разбавления или полная замена электролита новым.
В первом случае следует провести такие действия для каждой банки:
- Откачать по возможности максимальное количество электролитической жидкости с помощью резиновой груши или колбы;
- Внести в банку половину ее объема электролита с плотностью от 1,275 до 1,29 г на куб. см;
- Для перемешивания электролита на выводы подается нагрузка небольшой мощности, например при подключении обычной лампочки для автомобилей, или выдерживание на протяжении нескольких часов;
- При замере плотности следует определить нужный уровень. Если не было изменений, то в половину оставшегося объема следует внести еще электролит;
- Повторное перемешивание с замером;
С помощью подобных манипуляций следует довести до нужной плотности концентрацию серной кислоты в электролите.
При показателе индикатором значения плотности ниже 1,2 г на куб. см, требуется полная замена электролитической жидкости, поскольку подобным способом поднятие ее невозможно. Такой уровень в заряженном состоянии наводит на мысль о целесообразности операции.
см, требуется полная замена электролитической жидкости, поскольку подобным способом поднятие ее невозможно. Такой уровень в заряженном состоянии наводит на мысль о целесообразности операции.
Если батарее менее года, то процедура может увенчаться успехом, более старые элементы питания, скорее всего, реанимацию не переживут.
Полезное видео
Видеоинструкция по обслуживанию аккумулятора
Какой электролит заливать?
Для приготовления нового электролита требуется концентрированная кислота для аккумуляторов, которая продается с плотностью 1,835 – 1,84 г на куб. см. Разбавляется жидкость чистой дистиллированной водой, поскольку содержащиеся соли металлов в обычной проточной воде пагубно влияют на электроды АКБ.
Важно! Внесение дистиллята в кислоту строго запрещено. В результате таких действий возникает сильный нагрев, бурная реакция с разбрызгиванием вещества.
Поэтому добавлять следует кислоты в дистиллированную воду тонкой струйкой.
Для того чтобы развести аккумуляторную жидкость, следует проделать такие операции:
- По возможности использовать защитную одежду: защитные очки, химически устойчивую одежду и резиновые перчатки.
- Подготовить все ингредиенты и инструменты: кислоту, дистиллированную воду, ареометр, химически стойкую посуду,
- Рассчитать количество кислоты и дистиллированной воды для необходимого результата. В среднем в АКБ залито 2,6-3,7 литра раствора, но лучше разведение производить с расчетом на объем 4 литра;
- В устойчивую к кислотным воздействиям емкость наливается нужный объем дистиллята;
- Постепенно разбавляется дистиллированная вода кислотой с постоянным перемешиванием, чтобы плотные слои разводились равномерно, а не опускались на дно емкости;
- Ареометром замеряется плотность полученного раствора;
- При наличии показателя, близкого к требуемому значению, раствор должен настояться несколько часов для лучшего перемешивания.

Таблица плотностей электролита и соотношения дистиллята и кислоты
При получении слишком концентрированной жидкости, следует провести разбавление ее дистиллятом. При смешивании дистиллированной воды и аккумуляторной кислоты в процессе реакций выделяется тепло, которое будет опасным для электродов. Поэтому заливать в банки следует только остывший раствор.
Заключение
Срок службы аккумуляторной батареи ограничивается ее техническими характеристиками. Однако неправильное использование и хранение может существенно снизить этот показатель. Чтобы АКБ не изнашивалась стремительно, нужно следить за плотностью электролита и его уровнем.
В результате химических процессов повышение плотности раствора происходит из-за высокой температуры и естественных реакций окисления и восстановления. Поэтому следует доливать дистиллят. Сильное падение плотности требует полноценной замены электролитической жидкости. Важно соблюдать меры предосторожности при работе с емкостью, а также следовать четким инструкциям.
Вконтакте
Google+
Аккумуляторная серная кислота. Общая информация.
Кислота серная аккумуляторная.
Серная кислота — сильная двухосновная кислота. Представляет собой при нормальных условиях тяжёлую маслянистую жидкость без цвета и запаха.
Химическая формула: H2SO4
Молекулярная масса: 98,08 (по международным атомным массам 1971 г.)
Плотность вещества 1,8356 г/см3 .
Применение аккумуляторной серной кислоты.
Серная аккумуляторная кислота применяется для приготовления аккумуляторного электролита для свинцово-кислотных аккумуляторных батарей различного применения.
Сорта аккумуляторной серной кислоты.
Кислота серная аккумуляторная производится двух сортов, различающихся неодинаковым количеством примесей. Показатели состава и содержания примесей приведены в таблице 1.
Таблица 1. Допустимое содержание примесей в аккумуляторной серной кислоте.
|
Наименование показателя Массовая доля… |
Норма /не более |
|
|
Высший сорт |
1-й сорт |
|
|
ОКП 212111072000 |
ОКП 212111073009 |
|
|
— моногидрата (h4SО4), % |
92-94 |
92-94 |
|
— железа (Fe), %, |
0,005 |
0,010 |
|
— остатка после прокаливания, %, |
0,02 |
0,03 |
|
— окислов азота (N2O3), %, |
0,00003 |
0,0001 |
|
— мышьяка (As), %, |
0,00005 |
0,00008 |
|
— хлористых соединений (Сl), %, |
0,0002 |
0,0003 |
|
— марганца (Мn), %, |
0,00005 |
0,0001 |
|
— суммы тяжелых металлов в пересчете на свинец (Рb), %, |
0,01 |
0,01 |
|
— меди (Cu), %, |
0,0005 |
0,0005 |
|
— доля веществ, восстанавливающих KMnO4, см3 раствора с (1/5 KMnO4) = 0,01 моль/дм3, |
4,5 |
7 |
|
Удельный вес |
1,830 |
|
Документы, регламентирующие производство аккумуляторной серной кислоты.
ГОСТ 667-73 «Кислота серная аккумуляторная. Технические условия».
Тара для перевозки и хранения аккумуляторной серной кислоты.
При перевозке серной аккумуляторной кислоты могут быть использованы следующие ёмкости:
— специализированные железнодорожные цистерны для перевозки серной кислоты. Цистерны маркируются надписями «Аккумуляторная серная кислота», «Опасно»;
— контейнеры из нержавеющей стали марки ЭИ-448 по ГОСТ 5632-72;
— контейнеры, защищённые внутри фторопластом;
— специальные пластиковые контейнеры, 1куб. м., на деревянном или пластиковом поддоне в металлической обрешётке;
— ПЭТ бочки и канистры, вместимостью от 10 до т216 дм. куб.;
— стеклянные бутыли по 20 литров. Бутыли, как правило, помещаются в контейнеры для транспортировки и хранения. Бутыли закрываются стеклянными пробками с хорошо притертой поверхностью, навинчивающимися полиэтиленовыми или пластмассовыми крышками.
Свойства аккумуляторной серной кислоты.
Аккумуляторная серная кислота:
— пожаро- и взрывобезопасна;
— при соединении ее с водой, происходит бурная реакция с большим выделением тепла, паров и газов;
— аккумуляторная серная кислота очень токсична. Вещество второго класса опасности, по степени воздействия на организм человека. Предельно допустимая концентрация паров серной кислоты в воздухе рабочей зоны производственных помещений — 1 мг/м3
Техника безопасности при работе с аккумуляторной серной кислотой.
Перед работой с аккумуляторной серной кислотой необходимо изучить её свойства, ознакомиться с соответствующими инструкциями по технике безопасности, сдать необходимый экзамен. При работе необходимо пользоваться средствами защиты органов дыхания и зрения, иметь специальную защитную одежду и обувь, а так же перчатки.
В случае ожогов произвести необходимые действия по программе первой медицинской помощи и затем немедленно обратиться к врачу.
советы по подготовке, правила эксплуатации
Электрическая батарея автомобиля представляет собой перезаряжаемый аккумулятор, который обеспечивает электрической энергией двигатель при его запуске и позволяет функционировать всем системам транспортного средства. Работоспособность батареи определяется его выходным напряжением, которое в большей степени зависит от состава электролита для аккумуляторов.
Общая информация
Аккумуляторная батарея получила такое название потому, что она состоит из нескольких ячеек, которые располагаются одна за другой в ряд. Такое устройство является последовательным соединением электрических элементов в цепи, что позволяет увеличить выходное напряжение. Каждая ячейка батареи представляет собой закрытый сосуд, в котором расположены два электрода, погруженные в специальную жидкость — электролит, представляющий собой смесь серной кислоты и дистиллированной воды. Он выступает в качестве среды, обеспечивающей ионный обмен между электродами.
Положительные электроды — пластины, которые состоят из пентоксида свинца, а отрицательные электроды — пластины из активного свинца. Они объединяются и группируются с помощью контактных прослоек горизонтального и вертикального типа. Такая структура обеспечивает равномерное распределение электрического тока. Объединение положительных и отрицательных свинцовых пластин называется элементом. Как правило, отрицательные пластины имеют большую толщину.
Каждый элемент батареи отделяется тонкой прослойкой из пластика. Эта прослойка предотвращает возникновение короткого замыкания между рядом находящимися плюсом и минусом соседних элементов.
Между электродами и электролитом происходят электрохимические реакции, в результате которых поглощаются или выделяются электроны. Такие реакции создают разницу напряжений между электродами элемента.
На внешнюю часть корпуса аккумулятора выводятся две клеммы, с помощью которых он подсоединяется к электрической цепи. Эти клеммы расположены на верху корпуса, однако в некоторых батареях они делаются сбоку. В последнем случае возникает множество проблем, связанных с их расположением, в частности, боковые клеммы облегчают скопление паров электролита внутри батареи, что приводит к быстрому выходу из строя его рабочих элементов.
Эти клеммы расположены на верху корпуса, однако в некоторых батареях они делаются сбоку. В последнем случае возникает множество проблем, связанных с их расположением, в частности, боковые клеммы облегчают скопление паров электролита внутри батареи, что приводит к быстрому выходу из строя его рабочих элементов.
Клемма аккумулятора является либо положительной, либо отрицательной. Положительная клемма имеет больший размер, поэтому выполнить правильную установку батареи не составит никакого труда даже новичку. Если подсоединить неправильно аккумулятор, то есть перепутать плюс и минус, тогда можно повредить всю электрическую цепь.
Происходящие электрохимические реакции приводят к медленному износу активных элементов батареи, в частности, отрицательные электроды окисляются и становятся толще, а положительные электроды восстанавливаются и утончаются. По этой причине при покупке аккумулятора для автомобиля всегда следует обращать внимание на гарантийный срок службы устройства.
Аккумулятор может работать в ограниченном температурном диапазоне и плохо переносит низкие температуры, поэтому уход за ним состоит в периодических проверках напряжения на его клеммах и его механической целостности. Важно следить за наличием в батареи электролита для кислотных аккумуляторов и составом его.
Важно следить за наличием в батареи электролита для кислотных аккумуляторов и составом его.
Концентрация кислоты
Основным компонентом электролита автомобильной аккумуляторной батареи (АКБ) является концентрированная серная кислота. Но на чистой серной кислоте устройство работать не может, поэтому в составе автомобильного электролита также присутствует дистиллированная вода. Государственный стандарт ГОСТ 667–73 регулирует качество серной кислоты, поставляемой для АКБ. Важность соблюдения этого ГОСТа связаны с резким снижением срока службы устройства в случае использования грязной серной кислоты.
Плотность серной кислоты равна 1,84 г/мл, рабочее же значение плотности электролита составляет 1,3 г/мл. Следует знать, что при приготовлении электролита выделяется большое количество теплоты, поэтому не нужно забывать правило, что следует всегда лить кислоту в воду, и ни в коем случае наоборот.
Электролит, плотность которого лежит в пределе 1,07 — 1,30 г/мл, считается пригодным для работы.
Этому пределу плотности соответствует концентрация h4SO4 27−40%.
Правила эксплуатации
Свойства электролита достаточно чувствительны к смене температурного режима окружающей среды, поэтому в зонах с умеренным климатом рекомендуется проверять его состояние два раза в год: в конце осени и в конце весны.
Измерение плотности
Плотность является важной характеристикой кислотного электролита, состав которого определяет ее величину. Прибор, которым измеряется плотность электролита, называется ареометром, который можно купить в любом автомагазине. При его использовании следует учитывать температуру окружающей среды и связанный с ней поправочный коэффициент.
Следующая таблица демонстрирует поправочные коэффициенты к полученным показаниям ареометра в зависимости от температуры (градусы Цельсия):
- от -40 до -26: -0,04;
- от -25 до -11: -0,03;
- от -10 до +4: -0,02;
- от +5 до +19: -0,01;
- от +20 до +30: 0,00;
- от +31 до +45: +0,01.

Помимо ареометра, для записи измеренных результатов рекомендуется заранее приготовить чистый лист бумаги и карандаш. Проверку необходимо проводить в каждом элементе батареи отдельно. Следующие шаги объясняют порядок действий:
- Первым делом следует открыть каждую емкость в батарее, плотность электролита в которой должна быть измерена.
- Предназначенную для измерения часть ареометра нужно поместить в электролит.
- Грушей прибора следует забрать некоторую порцию электролита так, чтобы поплавок ареометра начал плавать.
- В месте соприкосновения специального стержня и жидкости следует смотреть настоящие показания измеряемой величины.
- Полученный результат записать, а затем провести аналогичные действия для оставшихся емкостей батареи.
Плотность является физической величиной, размерность которой определяется как г/см3. В случае электролита после проведенных измерений следует удостовериться, что ее колебания во всех элементах АКБ не превышают 0,2−0,3 г/см3. Если средняя величина плотности по всем емкостям АКБ лежит ниже установленного значения в паспорте, тогда необходимо зарядить аккумулятор.
Если средняя величина плотности по всем емкостям АКБ лежит ниже установленного значения в паспорте, тогда необходимо зарядить аккумулятор.
При уходе за аккумулятором и контроле плотности электролита необходимо иметь в виду температурный режим. Так, в холодное время года следует поддерживать более высокие значения этой величины (1,30 г/см3), так как она обеспечивает более низкую температуру замерзания жидкости. Например, если значение плотности лежит ниже 1,1 г/см3, то в электролите могут появляться кристаллики льда уже при температуре -6 °C. Летом же лучше снижать плотность заряженной батареи до уровня 1,23 г/см3, поскольку чем она ниже, тем дольше прослужит устройство.
Зимой при низких температурах воздуха рекомендуется снимать аккумулятор с автомобиля и заносить его в помещение, в котором следует проводить все контролирующие замеры электролитических параметров. Кроме того, для эксплуатации электроприбора в северных районах страны следует приобрести специальный контейнер-рубашку, который позволяет сохранять тепло корпуса АКБ.
Уровень жидкости
Еще одной ключевой характеристикой аккумуляторной батареи, за которой необходимо следить регулярно, является уровень электролита в каждом элементе. Согласно общим рекомендациям, он не должен быть ниже 1−1,5 см верхнего края пластин.
Перед измерением уровня электролита в каждой секции батареи следует поставить электроприбор на горизонтальную поверхность. После этого рекомендуется взять стеклянную трубку длиной 25−30 см и диаметром 5−6 мм, опустить ее на дно измеряемой банки, закрыть свободный конец трубочки большим пальцем, чтобы предотвратить спад жидкости в ней при вытягивании из банки, а затем вытянуть ее из электролита и любой линейкой измерить уровень.
Эту операцию можно провести с помощью обычного листа бумаги, который следует свернуть в трубочку и опустить на дно измеряемой емкости. При последующем измерении линейкой мокрого отпечатка на листе следует учесть величину погрешности, возникающую из-за капиллярного эффекта.
Если при измерениях обнаружен недостаток жидкости в какой-либо емкости батареи, тогда следует в нее добавить нужное количество дистиллированной воды.
Делать это следует осторожно, небольшими порциями, поскольку вода, попадая в кислоту, вызывает большое выделение теплоты и вскипание. Добавлять следует именно воду, а не электролит, в противном случае можно серьезно повредить электроприбор.
Подготовка электролита и батареи
Если старый аккумулятор вышел из строя и пришло время купить новый, то можно поступить двумя способами: во-первых, можно купить уже готовый залитый в АКБ электролит, во-вторых, можно приобрести сухозаправленную батарею и самостоятельно выполнить ее заливку. Первый способ рекомендуется для новичков, ко второму же методу следует прибегать, если прибор будет эксплуатироваться в каких-либо экстремальных условиях.
При подготовке раствора самостоятельно необходимо следующее:
- Канистра с дистиллятом, которая продается в каждом автомагазине, приобрести эту воду можно и в аптеке.
- Серная кислота h4SO4. Рекомендуется приобретать ее в разбавленном виде, то есть с плотностью 1,40 г/см3. Реже используется концентрированная кислота с плотностью 1,84 г/см3.
- Градуированная емкость, которую можно использовать, чтобы отмерять нужные порции жидкости.
- При приготовлении электролита его нужно будет мешать, поэтому следует запастись трубкой из химически инертного материала, например, из стекла или керамики.
- Резиновые перчатки, прозрачные очки, защитный фартук, старая одежда — основные средства индивидуальной защиты.
Во время приготовления раствора следует соблюдать элементарные правила химической безопасности, которые заключаются в добавлении воды в электролит не большими порциями, что может привести к вскипанию и разбрызгиванию во все стороны жидкости, а тонкой струей. При этом трубкой рекомендуется плавно перемешивать раствор.
Аккумуляторный электролит нужного состава готовится согласно инструкции на упаковке путем смешивания кислоты и дистиллята. В ряде случаев их объемы смешиваются в равных количествах. После завершения процедуры надо будет замерить плотность ареометром.
В различных моделях автомобилей используют АКБ разного объема, вариации которого составляют от 2,6 до 3,7 л. В любом случае электролит можно приготовить с запасом, а оставшийся раствор необходимо нейтрализовать, бросив в него несколько ложек пищевой соды.
Как только рабочий раствор подготовлен, его нужно залить во все емкости батареи. Использовать для этого нужно либо стеклянную воронку, либо стеклянную кружку с удобным носиком. Процесс заполнения банок прибора следует проводить аккуратно и не спеша.
Заполнение производят до уровня, когда свинцовые пластины поднимаются над поверхностью электролита на 1−1,5 см. Затем прибор оставляют на 3−4 часа, при этом плотность раствора может незначительно уменьшиться.
Через несколько часов после заправки АКБ заряжают. Выполняется это так: на корпусе батареи проверяется значение емкости в Ампер-часах, это число делится на 10, и полученную величину уже используют для установления тока зарядки. Например, если емкость батареи составляет 80 А*ч, тогда ток для ее зарядки равен 8 А. Заряжать следует в течение 4 часов, после чего замеряются значения плотности и уровня электролита, и если они соответствуют рабочим величинам, тогда аккумуляторная батарея готова к использованию.
Потери воды, расслоение кислот и поверхностный заряд
Ознакомьтесь с простыми рекомендациями по продлению срока службы свинцово-кислотных аккумуляторов при правильном использовании.
Кислотная стратификация
Электролит многослойной батареи концентрируется внизу, истощая верхнюю половину элемента. Кислотное расслоение происходит, если аккумулятор остается на низком уровне заряда (ниже 80 процентов), никогда не получает полного заряда и имеет неглубокие разряды. Поездка на автомобиле на короткие расстояния с включенными аксессуарами, ограничивающими мощность, способствует расслоению кислоты, поскольку генератор не всегда может подавать насыщенный заряд.Особенно подвержены кислотному расслоению большие роскошные автомобили. Это не дефект батареи как таковой, а связано с применением. На рисунке 1 показан обычный аккумулятор, в котором кислота равномерно распределена сверху вниз.
Рисунок 1: Нормальный аккумулятор. Кислота равномерно распределяется сверху вниз по батарее, обеспечивая хорошие общие характеристики. Предоставлено Cadex |
На рисунке 2 показана многослойная батарея, в которой концентрация кислоты мала сверху и повышена снизу. Легкая кислота наверху ограничивает активацию пластины, способствует коррозии и снижает производительность, в то время как высокая концентрация кислоты внизу заставляет батарею казаться более заряженной, чем она есть, и искусственно повышает напряжение холостого хода. Неравномерный заряд пластин снижает CCA (ток холодного пуска), и запуск двигателя происходит медленно.
Рисунок 2: Многослойная батарея. Концентрация кислоты небольшая вверху и высокая внизу. Это повышает напряжение холостого хода, и аккумулятор кажется полностью заряженным. Избыточная концентрация кислоты вызывает сульфатирование нижней половины пластин. Предоставлено Cadex |
Если дать батарее отдохнуть в течение нескольких дней, встряхнуть или наклонить батарею набок, это поможет решить проблему.Применение выравнивающего заряда путем повышения напряжения 12-вольтовой батареи до 16 вольт в течение 1-2 часов также помогает путем смешивания электролита посредством электролиза. Не увеличивайте дозировку сверх рекомендованного времени. Подзарядка применяется для поддержания полного заряда и предотвращения сульфатирования свинцово-кислотных аккумуляторов.
Не всегда можно избежать расслоения кислоты. В холодные зимние месяцы стартерные батареи большинства легковых автомобилей имеют уровень заряда 75 процентов. Зная, что работа двигателя на холостом ходу и движение в пробке недостаточно заряжает аккумулятор; периодически заряжайте аккумулятор с помощью внешнего зарядного устройства.Если это нецелесообразно, переключитесь на батарею AGM. AGM не страдает от расслоения кислоты и менее чувствителен к сульфатированию при недостаточной загрузке, чем версия с затоплением. AGM немного дороже залитой версии, но батарея должна работать дольше.
Поверхностный заряд
Свинцово-кислотные батареи медлительны и не могут быстро преобразовать сульфат свинца в свинец и диоксид свинца во время зарядки. Это замедленное действие приводит к тому, что большая часть активности заряда происходит на поверхностях пластин, что приводит к повышенному состоянию заряда (SoC) снаружи.
Аккумулятор с поверхностным зарядом имеет немного повышенное напряжение и дает ложные показания SoC на основе напряжения. Чтобы нормализовать состояние, включите электрические нагрузки, чтобы снять около 1 процента емкости батареи, или дайте батарее отдохнуть в течение нескольких часов. Включите фары на несколько минут. Поверхностный заряд — это не дефект аккумулятора, а обратимое состояние.
Простые рекомендации по продлению срока службы батареи
.Свинцово-кислотный аккумулятор— Простая английская Википедия, бесплатная энциклопедия
Свинцово-кислотный аккумулятор в автомобилеСвинцово-кислотная батарея — вторичный элемент, то есть перезаряжаемый. Это очень распространено в легковых и грузовых автомобилях. Он содержит пластины свинца и оксида свинца (IV) в растворе серной кислоты. Оксид свинца (IV) окисляет свинцовую пластину, создавая электрический ток.
Свинцово-кислотные батареи — самые дешевые перезаряжаемые батареи, которые могут производить много энергии. Однако они содержат токсичный свинец и должны быть переработаны.Это влажные клетки, и опасная кислота может вылиться наружу. Герметичные свинцово-кислотные батареи — это батареи, в которых серная кислота находится в геле, который остается внутри, даже когда аккумулятор перевернут.
Реакции:
- оксид свинца (IV) + серная кислота + дополнительные ионы водорода → сульфат свинца (II) + вода на катоде
- свинец + дополнительные ионы сульфата → сульфат свинца (II) на аноде
Эти реакции меняются на противоположные, когда аккумулятор заряжается.
- Влажная камера
- Стол аккумуляторов
Информация о свинцовых батареях — Battery University
Узнайте о различиях в семействе свинцово-кислотных продуктов и выясните, каковы их недостатки и преимущества.
Свинцово-кислотная батарея, изобретенная французским врачом Гастоном Планте в 1859 году, стала первой аккумуляторной батареей для коммерческого использования. Несмотря на свой преклонный возраст, химический состав свинца по-прежнему широко используется сегодня. Для его популярности есть веские причины; Свинцово-кислотный продукт надежен и недорог, исходя из цены за ватт.Есть несколько других аккумуляторов, которые поставляют большую часть энергии так же дешево, как свинцово-кислотные, и это делает их экономически выгодными для автомобилей, гольф-каров, вилочных погрузчиков, морских источников и источников бесперебойного питания (ИБП).
Сетка свинцово-кислотного аккумулятора изготовлена из свинцового сплава. Чистый свинец слишком мягкий и не поддерживает сам себя, поэтому для придания механической прочности и улучшения электрических свойств добавляют небольшие количества других металлов. Самые распространенные добавки — сурьма, кальций, олово и селен.Эти батареи часто называют «свинцово-сурьмянистыми» и «свинцово-кальциевыми».
Добавление сурьмы и олова улучшает глубокую цикличность, но это увеличивает потребление воды и обостряет необходимость выравнивания. Кальций снижает саморазряд, но положительная свинцово-кальциевая пластина имеет побочный эффект роста из-за окисления сетки при избыточном заряде. В современных свинцово-кислотных аккумуляторах также используются легирующие добавки, такие как селен, кадмий, олово и мышьяк, для снижения содержания сурьмы и кальция.
Свинцовая кислота тяжелая и менее долговечна, чем системы на основе никеля и лития при глубоком цикле.Полная разрядка вызывает напряжение, и каждый цикл разрядки / зарядки навсегда лишает аккумулятор небольшой емкости. Эти потери невелики, пока батарея находится в хорошем рабочем состоянии, но затухание увеличивается, когда производительность падает до половины номинальной емкости. Эта характеристика износа применима ко всем батареям в разной степени.
В зависимости от глубины разряда свинцово-кислотный аккумулятор для приложений глубокого цикла обеспечивает от 200 до 300 циклов разряда / заряда. Основными причинами его относительно короткого срока службы являются коррозия сетки на положительном электроде, истощение активного материала и расширение положительных пластин.Это явление старения ускоряется при повышенных рабочих температурах и при больших токах разряда. (См. BU-804: Как продлить срок службы свинцово-кислотных аккумуляторов)
Зарядка свинцово-кислотных аккумуляторов проста, но необходимо соблюдать правильные пределы напряжения. Выбор низкого предела напряжения защищает аккумулятор, но это снижает производительность и вызывает накопление сульфатации на отрицательной пластине. Предел высокого напряжения улучшает характеристики, но вызывает коррозию сетки на положительной пластине. Хотя сульфатирование можно обратить вспять, если вовремя отремонтировать, коррозия необратима.(См. BU-403: Зарядка свинцово-кислотных устройств.)
Свинцово-кислотные аккумуляторы не подходят для быстрой зарядки, и для большинства типов полная зарядка занимает 14–16 часов. Аккумулятор должен всегда храниться полностью заряженным. Низкий заряд вызывает сульфатирование — состояние, которое снижает производительность аккумулятора. Добавление углерода на отрицательный электрод уменьшает эту проблему, но снижает удельную энергию. (См. BU-202: Новые свинцово-кислотные системы.)
Свинцово-кислотный аккумулятор имеет средний срок службы, но он не зависит от памяти, как системы на основе никеля, и сохраняет заряд лучше, чем аккумуляторные батареи.В то время как NiCd теряет примерно 40 процентов своей запасенной энергии за три месяца, свинцово-кислотный саморазряд разряжается за один год. Свинцово-кислотный аккумулятор хорошо работает при низких температурах и превосходит литий-ионный при работе в отрицательных условиях. По данным RWTH, Аахен, Германия (2018), стоимость свинцово-кислотных аккумуляторов составляет около 150 долларов за кВтч, что является одним из самых низких показателей среди батарей.
Герметичный свинцово-кислотный
Первая герметизированная свинцово-кислотная кислота, не требующая обслуживания, появилась в середине 1970-х годов.Инженеры утверждали, что термин «герметичный свинцово-кислотный» был неправильным, потому что ни одна свинцово-кислотная батарея не может быть полностью герметичной. Для контроля вентиляции при напряженной зарядке и быстрой разрядке были добавлены клапаны, выпускающие газы при повышении давления. Вместо того, чтобы погружать плиты
.Формула серной кислоты — использование серной кислоты, свойства, структура и формула
Формула и структура: Химическая формула серной кислоты H 2 SO 4 , а ее молекулярная масса составляет 98,079 г / моль. Его химическая структура показана ниже. Атом серы связан с двумя атомами кислорода двойными связями и двумя гидроксильными группами (ОН) одинарными связями. Это дипротонная кислота, так как она может выделять два протона.
Прохождение: Серная кислота образуется естественным путем в результате окисления сульфидных минералов в горных породах.Разбавленная серная кислота также образуется в атмосфере в результате окисления диоксида серы (в результате сжигания топлива) в присутствии влаги, в конечном итоге выпадая в виде «кислотного дождя».
Получение: Серную кислоту получают в промышленных масштабах реакцией воды с триоксидом серы.
SO 3 + H 2 O → H 2 SO 4
Триоксид серы (SO 3 ) образуется в результате реакции диоксида серы и кислорода, катализируемой оксидом ванадия, в процессе контактного или камерного процесса.
Физические свойства: H 2 SO 4 представляет собой бесцветную или слегка желтоватую вязкую жидкость с резким запахом. Он имеет плотность 1,84 г / мл, температуру кипения 337 ° C и точку плавления 10 ° C. «Концентрированная» серная кислота на 98% содержится в воде и является наиболее стабильной формой. Многие другие концентрации с разными названиями доступны для различных целей. Аккумуляторная кислота составляет 29–32%, камерная кислота — 62–70%, а кислотная — 78–80%.
Химические свойства: Серная кислота — очень сильная дипротонная кислота.Он гигроскопичен и легко впитывает влагу из воздуха. Это мощный окислитель, вступающий в реакцию со многими металлами при высоких температурах. Концентрированный H 2 SO 4 также является сильным обезвоживающим агентом. Добавление воды к концентрированной серной кислоте является очень экзотермической реакцией и может привести к взрывам.
Применение: Серная кислота находит множество применений в различных отраслях промышленности, таких как переработка полезных ископаемых, переработка нефти, производство удобрений, очистка сточных вод и т. Д.Он также используется в производстве чистящих средств, красителей, пигментов, лекарств, моющих средств и взрывчатых веществ. Обычно он используется в качестве электролита в свинцово-кислотных аккумуляторах.
Опасность для здоровья / воздействие на здоровье: Концентрированный H 2 SO 4 является очень коррозионным и может серьезно повредить ткани при контакте. Как сильная кислота, окислитель, коррозионный агент и дегидратирующий агент, он более опасен, чем другие минеральные кислоты. При контакте с кожей вызывает сильные химические ожоги. Попадание в глаза может привести к необратимым повреждениям и слепоте.Проглатывание кислоты может даже привести к смерти.
.Информация об аккумуляторах: все, что вам нужно знать об аккумуляторах
Меню Поиск- Дом
- Новости
- Свяжитесь с нами
Поиск: Поиск
- Продукты
- Автомобильная промышленность
- Коммерческие автомобили
- Промышленное применение
- ИБП
- Телекоммуникации
- Возобновляемая энергия
- Пожарная безопасность и охрана
- Гольф и мобильность
- Аварийное освещение
- Накопитель энергии
- Уборка полов и доступ с воздуха
- Мотоцикл и силовой спорт
- Отдых, море и сад
- Зарядные устройства, тестеры и аксессуары
- Автомобильная промышленность
Диапазоны
- Обзор
- YBX9000 AGM
- YBX7000 EFB
- YBX5000
- YBX3000
- YBX1000
- Вспомогательное оборудование, резервное копирование и специалист
- классический
- Посмотреть все батареи
Информация
- Все, что вам нужно знать об аккумуляторах
- Как работает аккумулятор
- Общие сведения о спецификациях
- Серебряные кальциевые батареи
- Характеристики аккумулятора и диагностика неисправностей
- Тестирование батарей
- Здоровье и безопасность
- Видео
Новые технологии
- Разъяснение AGM и EFB
- Микрогибридные и гибридные автомобили
- Вспомогательные и резервные батареи
- Инструмент настройки Yu-Fit
- Предупреждение о замене батареи
Загрузки
- Руководства по применению Брошюры, краткие формы и руководства линейки
- Уход за батареями и тестирование
- Паспорта безопасности
- Таблица перекрестных ссылок
Гарантия качества
- Гарантия для автомобилей и мотоциклов
- Промышленная гарантия
- Аккредитация
- OE Родословная
- Заявление о BER
- Политика возврата отработанной батареи
- Служба утилизации и вывоза аккумуляторных батарей
- Коммерческие автомобили
Диапазоны
- Обзор
- YBX 1000 SHD
- YBX 3000 SHD
- YBX 5000 SHD
- YBX 7000 EFB
- Pro Spec — глубокий цикл
- классический
- Посмотреть все
Информация
- Все, что вам нужно знать об аккумуляторах
- Как работает аккумулятор
- Общие сведения о спецификациях
- Серебряные кальциевые батареи
- Характеристики аккумулятора и диагностика неисправностей
- Тестирование батарей
- Здоровье и безопасность
- Видео
Новые технологии
- Разъяснение AGM и EFB
- Микрогибридные и гибридные автомобили
- Предупреждение о замене батареи
Загрузки
- Руководства по применению Брошюры, краткие формы и руководства линейки
- Уход за батареями и тестирование
- Паспорта безопасности
- Таблица перекрестных ссылок
Гарантия качества
- Гарантия для автомобилей и мотоциклов
- Промышленная гарантия
- Аккредитация
- OE Родословная
- Заявление о BER
- Политика возврата отработанной батареи
- Служба утилизации и вывоза аккумуляторных батарей
- Промышленное применение
Диапазоны
- Обзор
- НП ВРЛА
- НПЛ VRLA
- НПХ ВРЛА
- НПВ VRLA
- NPC VRLA
- РЭ VRLA
- ОБНОВЛЕНИЕ VRLA
- REC VRLA
- SW — VRLA
- SWL VRLA
- EN VRLA
- ЭНЛ ВРЛА
- Передний терминал ENL VRLA
- FXH VRLA
- Pro Spec Deep Cycle
- SLR VRLA глубокого цикла
- LIM Литий-ионный
- Ю-Лайт
- Посмотреть все
Информация
- Golf & Mobility Battery Guidance
- Режим ожидания и циклические определения
- Руководство по установке, вводу в эксплуатацию и техническому обслуживанию
- Циклический VRLA Производительность и срок службы
- Видео
- Калькулятор промышленных размеров
Загрузки
- Руководства по применению Брошюры, краткие формы и руководства линейки
- Уход за батареями и тестирование
- Паспорта безопасности
- Таблица перекрестных ссылок
Гарантия качества
- Гарантия для автомобилей и мотоциклов
- Промышленная гарантия
- Аккредитация
- OE Родословная
- Заявление о BER
- Политика возврата отработанной батареи
- Служба утилизации и вывоза аккумуляторных батарей
- ИБП
Диапазоны
- НП VRLA
- НПЛ VRLA
- НПХ ВРЛА
- НПВ VRLA
- РЭ VRLA
- ОБНОВЛЕНИЕ VRLA
- SW — VRLA
- SWL VRLA
- EN VRLA
- ЭНЛ ВРЛА
- Передний терминал ENL VRLA
- LIM литий-ионный
Информация
- Golf & Mobility Battery Guidance
- Режим ожидания и циклические определения
- Руководство по установке, вводу в эксплуатацию и техническому обслуживанию
- Видео
Загрузки
- Руководства по применению Брошюры, краткие формы и руководства линейки
- Уход за батареями и тестирование
- Паспорта безопасности
- Таблица перекрестных ссылок
Гарантия качества
- Гарантия для автомобилей и мотоциклов
- Промышленная гарантия
- Аккредитация
- OE Родословная
- Заявление о BER
- Политика возврата отработанной батареи
- Служба утилизации и вывоза аккумуляторных батарей
- Телекоммуникации
Диапазоны
- НП VRLA
- НПЛ VRLA
- РЭ VRLA
- ОБНОВЛЕНИЕ VRLA
- SW — VRLA
- SWL VRLA
- EN VRLA
- ЭНЛ ВРЛА
- ENL VRLA Передний терминал
- FXH VRLA
- LIM Литий-ионный
Информация
- Golf & Mobility Battery Guidance
- Режим ожидания и циклические определения
- Руководство по установке, вводу в эксплуатацию и техническому обслуживанию
- Видео
Загрузки
- Руководства по применению Брошюры, краткие формы и руководства линейки
- Уход за батареями и тестирование
- Паспорта безопасности
- Таблица перекрестных ссылок
Гарантия качества
- Гарантия для автомобилей и мотоциклов
- Промышленная гарантия
- Аккредитация
- OE Родословная
- Заявление о BER
- Политика возврата отработанной батареи
- Служба утилизации и вывоза аккумуляторных батарей
- Возобновляемая энергия
Диапазоны
- НПЛ VRLA
- NPC VRLA
- REC VRLA
- ЭНЛ ВРЛА
- Передний терминал ENL VRLA
- FXH VRLA
- SLR VRLA глубокого цикла
- LIM литий-ионный
Информация
- Golf & Mobility Battery Guidance
- Режим ожидания и циклические определения
- Руководство по установке, вводу в эксплуатацию и техническому обслуживанию
- Видео
Загрузки
- Руководства по применению Брошюры, краткие формы и руководства линейки
- Уход за батареями и тестирование
- Паспорта безопасности
- Таблица перекрестных ссылок
Гарантия качества
- Гарантия для автомобилей и мотоциклов
- Промышленная гарантия
- Аккредитация
- OE Родословная
- Заявление о BER
- Политика возврата отработанной батареи
- Служба утилизации и вывоза аккумуляторных батарей
- Противопожарная охрана
Диапазоны
- НП VRLA
- НПЛ VRLA
- РЭ VRLA
Информация
- Golf & Mobility Battery Guidance
- Режим ожидания и циклические определения
- Руководство по установке, вводу в эксплуатацию и техническому обслуживанию
- Видео
Загрузки
- Руководства по применению Брошюры, краткие формы и руководства линейки
- Уход за батареями и тестирование
- Паспорта безопасности
- Таблица перекрестных ссылок
Испытания свинцово-кислотных батарей — Battery University
Откройте для себя разработки в области неинвазивных технологий быстрого тестирования.
В тестерах аккумуляторов недостатка нет, но большинству недостает точности. Емкость, главный индикатор работоспособности батареи, сложно получить на лету. Утверждение, что тестер аккумуляторов, измеряющий внутреннее сопротивление, также дает оценку емкости, вводит в заблуждение. Рекламные функции, выходящие за рамки возможностей оборудования, сбивают с толку отрасль, заставляя поверить в то, что сложные тесты можно проводить с помощью основных методов.Приборы, основанные на сопротивлении, могут идентифицировать умирающую или разряженную батарею — тоже самое делает пользователь. Продавцы часто сознательно завышают возможности тестеров аккумуляторов. Это похоже на рекламу шампуня, который обещает отрастить пышные волосы на лысой голове мужчины.
Без надежных тестовых устройств тестирование аккумуляторов превращается в догадки, в результате чего хорошие батареи заменяются слишком рано, а слабые — выдаются из строя, а вскоре после проверки они выходят из строя в дороге. Отсутствие точного тестирования батареи также приводит к ненужной замене батареи в рамках гарантийной программы.Изучение гарантийных возвратов показывает, что менее 10 процентов этих батарей имеют производственный брак. Большинство ошибок возникает по вине пользователя.
Проблема возникает при оценке батареи в рамках обычного обслуживания до того, как станет заметным снижение производительности. Такой тест эффективен только при включении измерения емкости. Емкость контролирует накопление энергии, управляет временем работы и прогнозирует окончание срока службы. С другой стороны, внутреннее сопротивление отвечает за мощность для запуска двигателя и выдачу высокого тока под нагрузкой по запросу.Снимок, сделанный с помощью тестера CCA на стартерной батарее, относится только к состоянию резистивной батареи. Лучшие электролиты и коррозионно-стойкие электродные материалы обеспечивают низкое сопротивление современных батарей на протяжении большей части их срока службы. Отказ из-за повышенного сопротивления стал редким и может развиться только в конце жизни. (См. BU: 901: Основы тестирования батарей.)
В отличие от измерений напряжения, тока и омических сопротивлений, не существует универсального прибора, который мог бы считывать емкость каждой батареи, которая идет в комплекте.Существует три распространенных концепции тестирования: скалярное, векторное и EIS со сложным моделированием (Spectro ™).
Скаляр — самый простой из трех. Он берет показания батареи и сравнивает их с эталонным значением, которое часто является резистивным значением. Большинство одночастотных тестеров проводимости переменного тока, измеряющих CCA, основаны на скалярной концепции.
Векторный метод применяет сигналы разных токов или возбуждает батарею с разными частотами, а затем оценивает результаты по заранее заданным векторным точкам для исследования батареи в различных условиях нагрузки.Это добавляет сложности, а дополнительные преимущества незначительны.
Spectro ™ сканирует аккумулятор с частотным спектром, как если бы он фиксировал топографию ландшафта, и сравнивает отпечаток с матрицей для оценки емкости аккумулятора, CCA и SoC. Spectro ™ обещает самый глубокий анализ батареи, но он также и самый сложный. (См. Также BU-904: Как измерить емкость.) На рис. 1 представлены три метода тестирования батарей.
| Тип | Возбуждение | Приложения | Результатов |
|---|---|---|---|
| Скаляр | Единая опорная точка; импульсы или одночастотное возбуждение | Автомобильная, стационарная; простой, часто используемый | Напряжение, CCA, внутреннее сопротивление, без нагрузки |
| Вектор | Множественные частоты, токи; сравнивается с вектором | Автомобильная, стационарная; реже используется | Как указано выше.Более сложный с предельной прибылью |
| Spectro ™ | Сочетает EIS со сложным моделированием; объединяет данные для определения емкости, CCA, SoC | Свинцовые и литиевые батареи | Обеспечивает CCA, емкость и SoC с соответствующими матрицами |
Рисунок 1: Методы сбора данных для экспресс-тестирования аккумуляторов . В таблице сравниваются скалярные, векторные и Spectro ™, сочетающие спектроскопию электрохимического импеданса (EIS) со сложным моделированием.
Матрица
Матрица — это многомерная справочная таблица, с которой сравниваются показания. Распознавание текста, идентификация отпечатков пальцев и визуализация работают по аналогичному принципу. При анализе батарей матрицы в основном используются для оценки емкости; тем не менее, CCA и состояние зарядки также выигрывают от использования матрицы.
Spectro правильно предсказывает емкость 8 из 10 аккумуляторов и 9 из 10 для CCA. Объединение этих двух классификаций дает значительный im
.Какая кислота в аккумуляторе автомобиля и для чего нужен электролит
Многие автолюбители задают себе вопрос о том, какая кислота залита в аккумуляторе автомобиля. По незнанию высказываются различные неверные предположения. Кто-то говорит, что там соляная кислота. Некоторые считают, что там вода. Пора внести ясность в этот вопрос. В свинцово-кислотном аккумуляторе автомобиля залита серная кислота. Если выражаться совсем точно, то залит раствор серной кислоты в дистиллированной воде. Этот раствор получил название электролит.
Содержание статьи
Применение серной кислоты и её сорта
Вообще, в качестве электролита в некоторых видах автомобильных аккумуляторов может использоваться щёлочь. Например, никель-кадмиевый или никель-железный тип АКБ. Есть ещё группа гелевых аккумуляторов AGM и GEL, где электролит находится в связанном состоянии. Но это тот же раствор серной кислоты. Просто он либо переведён в гелеобразное состояние с помощью добавок (GEL), либо им пропитано стекловолокно (AGM). Наиболее распространёнными на сегодняшний день остаются свинцово-кислотные автомобильные аккумуляторы с жидким электролитом. Поэтому речь пойдёт именно о водном растворе серной кислоты, предназначенном для заливки в АКБ.
Электролит
Дистиллированная вода
Серная кислота используется в самых разных отраслях народного хозяйства. К примеру, с её помощью очищается поверхность металла перед нанесением покрытия, она используется при приготовлении различных синтетических красителей. Кроме того, серная кислота востребована в сфере производства удобрений, взрывчатки, фармакологической промышленности, переработке нефти.
Серная кислота нашла широкое применение при производстве свинцово-кислотных аккумуляторов для автомобилей. Концентрация кислоты в электролите составляет 30-35 процентов (вес.). Остальное дистиллированная вода. Использовать обычную водопроводную воду нельзя, поскольку в ней содержатся соли различных металлов. Их попадание в аккумулятор автомобиля значительно сократит срок его службы.
В бытовой сфере концентрации Н2SO4 в 30 процентов достаточно, но в сфере производства часто используется серная кислота более высокой концентрации. Концентрированную серную кислоту получают в две стадии. На первой стадии концентрация доводится до 70 процентов, а затем увеличивают до 98 процентов. Серная кислота такой концентрации наиболее пригодна для последующего хранения. Возможно, получение концентрации 99 процентов, но в дальнейшем из-за потери SO3 она снижается до 98,3 процента.
Существуют основные сорта серной кислоты, которые перечислены ниже:
- Башенная или нитрозная. Концентрация 75 процентов. Плотность этого сорта составляет 1,67 гр/см3. Название этот сорт получил из-за метода производства в футерованных башнях нитрозным способом. Обжиговый газ с двуокисью серы (SO2) обрабатывается нитрозой (H2SO4 с добавками оксидов азота). В ходе химической реакции получается оксиды азота и кислота. При этом оксиды постоянно циркулируют в производственном цикле;
- Контактная. Концентрация от 92,5 до 98 процентов. Плотность сорта составляет 1,837 гр/см3. Этот сорт также производится из обжигового газа, в котором содержится двуокись SO2. В ходе реакции происходит ее окисление до SO3 при контакте с твёрдым катализатором из ванадия;
- Сорт Олеум. Концентрация 104,5 процента. Плотность составляет 1,897 гр/см3. Сорт представляет собой раствор SO3 в серной кислоте (H2SO4). Соотношение SO3 — 20 процентов, H2SO4 — 104,5 процента;
- Высокопроцентный олеум. Концентрация 114,6 процента, а плотность 2,002 гр/см3;
- Аккумуляторная. Концентрация от 92 до 94 процента, а плотность 1,835 гр/см3.
Вернуться к содержанию
Процессы, происходящие в АКБ с участием электролита
Работа свинцово-кислотного автомобильного аккумулятора основывается на электрохимических процессах, которые протекают с участием электролита. Аккумулятор автомобиля состоит из положительных и отрицательных пластин, погруженных в водный раствор серной кислоты. Положительные и отрицательные пластины имеют токоотводящие решётки из свинца с различными добавками в зависимости от типа аккумулятора.
На решётках положительных электродов нанесён красновато-коричневый диоксид свинца (PbO2). На отрицательных электродах — сероватый порошок свинца (Pb). Электрические характеристики аккумулятора напрямую зависят от плотности электролита. Для понимания назначения электролита нужно рассмотреть основные процессы, происходящие в аккумуляторе автомобиля.
При разряде аккумулятор на положительном электроде (аноде) идёт следующая реакция:
PbO2 + SO42− + 4H+ + 2e− -> PbSO4 + 2H2O
На отрицательном электроде (катоде) протекает такой процесс:
Pb + SO42− − 2e− ->PbSO4
При заряде АКБ эти реакции протекают в обратном направлении.
Электролит в свинцово-кислотном автомобильном аккумуляторе имеет разную плотность в зависимости от степени заряженности АКБ. Как уже говорилось выше, концентрированная кислота аккумуляторного сорта имеет плотность 1,835 гр/см3. Плотность электролита на заряженном аккумуляторе лежит в диапазоне 1,127─1,300 гр/см3. При разрядке аккумулятора автомобиля в результате электрохимической реакции из электролита расходуется серная кислота и его плотность падает. Пока через батарею проходит ток разряда кислота рядом с электродами расходуется в результате вышеописанной реакции. Идёт диффузия H2SO4 из объёма к электродам. Таким образом, поддерживается напряжение на выводах аккумулятора.
В начале разрядки процесс диффузии кислоты в электроды. Это объясняется тем, что в активной массе электродов поры ещё не забиты сульфатом. По мере того, как на них образуется слой сульфата и забивает поры, процесс диффузии притормаживается. В теории процесс разряда может идти до того момента, пока электролит не превратится в воду. Но на практике разряд идёт до тех пор, пока плотность не опуститься до значения 1,15 гр/см3. К моменту падения плотности до 1,15 гр/см3 выделяется столько сульфата свинца, что его хватило для закупоривания активной массы пластин. По плотности электролита можно судить о степени заряженности АКБ. Для этого можно использовать таблицу, представленную ниже.
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
|---|---|---|---|---|
| 1,11 | 11,7 | 8,4 | 0 | -7 |
| 1,12 | 11,76 | 8,54 | 6 | -8 |
| 1,13 | 11,82 | 8,68 | 12,56 | -9 |
| 1,14 | 11,88 | 8,84 | 19 | -11 |
| 1,15 | 11,94 | 9 | 25 | -13 |
| 1,16 | 12 | 9,14 | 31 | -14 |
| 1,17 | 12,06 | 9,3 | 37,5 | -16 |
| 1,18 | 12,12 | 9,46 | 44 | -18 |
| 1,19 | 12,18 | 9,6 | 50 | -24 |
| 1,2 | 12,24 | 9,74 | 56 | -27 |
| 1,21 | 12,3 | 9,9 | 62,5 | -32 |
| 1,22 | 12,36 | 10,06 | 69 | -37 |
| 1,23 | 12,42 | 10,2 | 75 | -42 |
| 1,24 | 12,48 | 10,34 | 81 | -46 |
| 1,25 | 12,54 | 10,5 | 87,5 | -50 |
| 1,26 | 12,6 | 10,66 | 94 | -55 |
| 1,27 | 12,66 | 10,8 | 100 | -60 |
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
Полностью заряженный элемент АКБ автомобиля выдаёт напряжение 2,5─2,7 вольт без нагрузки на выводах. При подключении нагрузки напряжение проседает до 2,1 вольта за несколько минут. За это время успевает сформироваться слой PbSO4 на поверхности отрицательных электродов. То есть, напряжение одного элемента на подключённой к автомобилю АКБ составляет примерно 2,15 вольта.
Если разряжать аккумулятор автомобиля небольшим током (10 процентов от номинальной ёмкости), то через час разрядки напряжение элемента снижается до 2 вольт. Это происходит из-за того, что в этом момент быстро формируется большое количество PbSO4, который забивает поры активной массы. В результате растёт внутреннее сопротивление элементов АКБ и падает концентрация электролита. Через некоторое время процесс разрядки выходит на прямую (см. график).
График разрядки аккумулятора
Эта прямая соответствует балансу плотностью электролита около электродов и в остальном объёме. Постепенно кислота поступает из объёма к электродам и вступает в реакцию с выделением сульфата свинца. Плотность электролита постепенно снижается, а напряжение падает медленнее, чем на начальной стадии. И на конечной стадии, когда активная масса блокируется образовавшимся сульфатом свинца, реакция замедляется и напряжение быстро падает.
Вернуться к содержанию
Контроль за состоянием электролита в АКБ?
От владельца автомобиля требуется периодически контролировать уровень электролита в аккумуляторе и его плотность. Для контроля уровня электролита можно использовать стеклянную трубочку. Если её под рукой нет, то можно использовать прозрачный пластиковый корпус от старой шариковой ручки. Для измерения уровня электролита отворачиваете пробки банок батареи и погружаете трубочку до пластин. Затем с верхнего конца плотно зажимаете пальцем и поднимаете. Уровень электролита в трубочке должен составлять 10─12 миллиметров.
В случае нехватки электролита долейте дистиллированной воды до необходимого уровня. Лучше покупайте дистиллированную воду в аптеке. В автомобильных магазинах под видом дистиллированной воды часто продают обычную водопроводную. Выше требуемого уровня воды также заливать не следует. В необслуживаемых автомобильных аккумуляторах (ссылка на материал) доливка дистиллированной воды не требуется. У них сниженный расход воды и они, как правило, имеют крышку с системой рециркуляции электролита.
Внимание! Не допускайте эксплуатации аккумуляторной батареи с уровнем электролита ниже верхней части пластин. Это значительно сокращает срок его службы.
Для того, чтобы измерить плотность Вам потребуется ареометр. Это приспособление представляет собой запаянную стеклянную трубку, в которой находиться ртуть или дробь. На верхнем конце ареометра имеется градуированная шкала. Диапазон измерений плотности 1,100─1,300 гр/см3. Ареометр помещён в разборную колбу с грушей.
Ареометр
Вам нужно опустить нижнюю часть в банку и набрать электролита. После этого вынимаете и смотрите, на каком значении находится уровень электролита. Сам ареометр будет плавать в электролите наподобие поплавка. На некоторых моделях ареометров шкала со значениями может быть заменена надписями «Полный заряд», «Половина», «Разряжен».
Вернуться к содержанию
Как поднять плотность электролита?
Выше уже говорилось о том, что в результате гидролиза воды и нагрева АКБ под капотом уровень электролита постепенно уменьшается и растёт его плотность. Поэтому периодически нужно доливать дистиллированной воды. А что, если плотность электролита на заряженном аккумуляторе автомобиля, наоборот, меньше нормы (1,275 гр/см3)? Тогда нужно поднять концентрацию кислоты.
Внимание! Во время работ с кислотой одевайте резиновые перчатки и защитные очки. Если вы будете самостоятельно разводить электролит из концентрированной кислоты и дистиллированной воды, помните, что нельзя наливать воду в кислоту. В этом случае начинается реакция гидратации с выделением большого количества тепла. В результате вода закипает и провоцирует брызги кислоты, что очень опасно. Поэтому при разбавлении нужно лить кислоту в воду.
При поднятии плотности электролита может быть два варианта. Если средняя плотность по всем банкам не ниже 1,2 гр/см3, то нужно поднять плотность постепенным разбавлением.
Для каждой из банок нужно проделать следующие действия:
- Откачиваете как можно больше электролита из банки. Для этого можно использовать резиновую грушу или ту же колбу. После этого в банку заливаете электролит (плотность 1,275─1,29 гр/см3) половину откачанного объёма;
- Для того чтобы электролит перемешался, можно дать на выводы нагрузку (например, подключить автомобильную лампочку) или просто подождать некоторое время;
- Затем делаете замер плотности. Если она не поднялась до нужного уровня, то заливаете электролит в половину от оставшегося объема;
- Перемешивание и снова замер;
- Доводите плотность кислоты до требуемого уровня.
Если плотность электролита ниже 1,2 гр/см3, то здесь уже нужно его менять полностью. То есть, сливать старый и заливать новый, требуемой плотности. Но, если электролит имеет такую низкую плотность в заряженном состоянии, то возникают сомнения в целесообразности его дальнейшего использования. В этом случае электролит имеет смысл менять только если АКБ относительно новая (до года). Иногда встречаются аккумуляторы автомобиля с такой плотностью электролита прямо из магазина. Если это уже отработавшая несколько лет батарея, то лучше купить новую. При утилизации аккумуляторов отработавший электролит также идет на переработку.
Вернуться к содержанию
Что мы узнали?
Из этой статьи читатели должны были узнать о том, какая кислота залита в аккумулятор автомобиля, какую плотность она должна иметь. Отдельно были рассмотрены химические реакции, проходящие в автомобильном аккумуляторе с участием электролита. Также были даны рекомендации по поддержанию уровня и плотности электролита и приспособлениях, которые для этого требуются. Если у вас остались вопросы или есть пожелания, пишите их в комментариях.
Вернуться к содержанию
Опрос
Примите участие в опросе!
Загрузка …Вернуться к содержанию
Какая кислота в аккумуляторе автомобиля: состав, характеристики
Длительный срок службы АКБ во многом зависит от состояния залитого электролита. Последний представляет собой кислотно-водный раствор. Чтобы контролировать его качество надо знать и какая кислота в аккумуляторе автомобиля, и её свойства. Это может пригодиться при покупке сухозаряженных источников питания, когда надо самостоятельно определяться с заливаемой жидкостью. Но особенно этот вопрос актуален для районов с экстремальными климатическими условиями.
Название и роль кислоты электролита
Источник энергии фактически является стандартной батареей. Внутри её находятся анод и катод, а также аккумуляторная жидкость или электролит. Последний представлен раствором кислоты с дистиллированной водой в процентном соотношении 30 к 70, соответственно. Такая пропорция компонентов обеспечивает наиболее эффективное взаимодействие жидкости со свинцовыми пластинами.
Обычная вода содержит примеси, уменьшающие срок службы батареи. А какая кислота в аккумуляторе автомобиля обеспечит появление тока? Та, что вступает в реакции обмена с разными металлами и оксидами, которые необходимы для функционирования батареи. Самым активным из подобных веществ является триоксид серы или ангидрид с химической формулой h3SO4. Более известное и распространённое среди обывателей название — серная кислота.
Когда подключается внешняя нагрузка, тогда взаимодействие жидкости со свинцом и оксидами приводит к необходимым окислительно-восстановительным реакциям. Они противоположны при заряде и разряде батареи. Ток возникает за счёт выделения электронов из свинца положительного элемента, которые принимает оксид отрицательной пластины. А передача заряженных частиц осуществляется благодаря действию раствора, который заливается в батарею.
Основные процессы, протекающие при разряде
На контактах АКБ происходят следующие химические процессы:
- на катоде восстанавливается оксид свинца;
- тратится триоксид серы;
- появляется вода;
- на аноде образуется окись металла.
Получается, что во время реакции кислоту заменяет более лёгкая вода. В результате плотность аккумуляторной жидкости падает. При заряде процессы идут в обратном направлении. После этого под действием возникающего тока начинается электролиз, то есть распад на водород и кислород. Происходит их выделение в газообразной форме. Из-за этого раствор начинает кипеть, так как активно выходят распавшиеся компоненты. Вещества покидают состав смеси, не возвращаясь обратно. Плотность электролита повышается, так как оставшаяся кислота более тяжёлая. Чтобы восстановить первоначальные свойства приходится доливать дистиллированную воду.
Электролит и его характеристики
Параметры растворов определяют потери энергии и даже условия эксплуатации машин, то есть рабочую температуру. Нормативно характеристики регулируются стандартом ГОСТ 667-73. В большей степени физико-химические свойства зависят от пропорций содержащихся компонентов. Плотность раствора определяется соотношением кислоты и воды. Именно она является самым важным свойством электролитов для аккумуляторов. Эта величина должна укладываться в пределы от 1,07 до 1,3 г/мл. Изменение концентрации кислоты поднимает или снижает порог замерзания. От неё же зависит электрическая проводимость, которая обратно пропорциональна сопротивлению АКБ. Обледенение ведёт к повреждению и полному разрыву банок в автомобильных аккумуляторах. При низких температурах плотность рабочей смеси рекомендуется повышать до 1,31 г/см³. С точки зрения электропроводности, это не самый лучший показатель. Но уменьшение может вызвать замерзание жидкости. Оптимальная величина с минимальным сопротивлением соответствует комнатной температуре и составляет 1,23 г/см³. Какую кислотность выбирать для идеального баланса между потерями энергии и соответствия конкретным климатическим условиям описано в таблице.
Температура и рекомендуемая плотность
| Среднемесячная температура, 0С | Время года | Плотность электролита, г/см³ |
| от -50 до -30 | зима | 1,28 |
| от -50 до -30 | лето | 1,24 |
| от -30 до -15 | круглый год | 1,27 |
| от -15 до -8 | круглый год | 1,24 |
| от -8 до +4 | круглый год | 1,20 |
| от -15 до +4 | круглый год | 1,22 |
Таблица 1. Зависимость плотности электролита от температуры зимой и летом.
Важно! Когда используется раствор с оптимальными для определённого времени года параметрами, тогда срок эксплуатации источника питания будет значительно продлён. Дело в том, что чрезмерно концентрированная смесь, залитая в тёплое время года, негативно, даже разрушительно влияет на автомобильный аккумулятор. Высокая плотность не только увеличивает потери энергии. Серный ангидрид до такой степени активное и едкое вещество, что он способен полностью разрушить электроды.
Изменение плотности раствора
Если снизить кислотность можно добавлением воды, то с увеличением так не получится. Плотность жидкости, залитой в аккумулятор, регулируется степенью заряженности батареи. Чем вторая величина выше, тем больше первая. Это объясняется тем, что по окончании окислительных и восстановительных реакций нередко происходит распад воды на составляющие в газообразном состоянии. То есть она теряется, а повышается концентрация кислоты в электролите. С помощью заряда избавляются от недостатка плотности. Если же и это не помогает — используют корректирующий электролит.
Соотношение заряда и плотности электролита
| Плотность при 25°С, г/см. куб. | Степень заряженности, % |
| 1,27 | 100 |
| 1,23 | 75 |
| 1,21 | 62,5 |
| 1,19 | 50 |
| 1,15 | 25 |
| 1,13 | 12,56 |
| 1,12 | 6 |
| 1,11 | 0 |
Таблица 2. Зависимость плотности электролита от величины заряда аккумуляторной батареи.
Присадки
Рынок предлагает огромное количество различных добавок, которые заливают в батарею для повышения качества электролита. Производители обещают улучшение запуска в морозы, увеличение срока службы, восстановление работоспособности АКБ и повышение энергоёмкости. Основное их действие — это десульфатация, но не настолько сильная, как заверяет реклама. Остальное не имеет достаточного подтверждения. Состав присадок редко раскрывают. Чаще всего это сульфаты или фосфаты металлов. Встречаются и средства из органических соединений. Причём вторые добавляют к аккумуляторной жидкости вместе с первыми. Для поддержания наилучшего состояния АКБ достаточно убирать его в период сильного похолодания в тёплое помещение или подзаряжать. Но это подойдёт, если говорить о регионах с умеренным климатом. Когда речь идёт о работе в экстремальных температурах, выгоднее может оказаться приобретение сухозаряженной батареи. Владелец сможет самостоятельно заливать электролит, максимально подходящий к условиям эксплуатации. На видео ниже показано, как из электролита получить серную и соляную кислоты. https://youtu.be/DTUom2xCh7M
состав и свойства — Информация
Пластиковый корпус и два контакта для подключения проводов. Именно так представляется автомобильный аккумулятор большинству из современных владельцев авто. Однако чтобы эксплуатировать его максимально эффективно, безопасно и без неожиданных сюрпризов, о батарее стоит знать немного больше.
Сегодня речь пойдет о столь важной составляющей конструкции авто и мото аккумуляторов, как электролит. Он представляет собой раствор серной кислоты, которая считается, пожалуй, одним из ключевых химических соединений в мире. Это обусловлено широким спектром ее применения. Раствор серной кислоты продается под различными наименованиями, которые зависят от степени крепости, а также уровня чистоты. Приведем несколько распространенных примеров:
- Камерная кислота – раствор серной кислоты с водой в пропорции от 60:40 до 70:30.
- Башенная кислота – раствор с соотношением от 75:25 до 82:18.
- Купоросное масло с содержанием серной кислоты до 97%.
- 100% серная кислота – моногидрат.
Если говорить о максимальной крепости, получаемой способом выпаривания, то этот параметр может достигать 98,5%. Однако для заправки аккумуляторных батарей ключевое значение приобретает чистота растворов купоросного масла с химической точки зрения.
Отметим также, что концентрированной серной кислотой называется совершенно прозрачная жидкость, не имеющая ни цвета, ни запаха. Она обладает консистенцию легкого масла. Ее удельный вес составляет 1б84 при температуре 15°С. В ней содержится примерно 95% серной кислоты. Концентрат может смешиваться с водой в любой пропорции. Изготавливая электролит в бытовых условиях, следует помнить, что смешивание воды и кислоты вызывает выделение значительного количества тепла. Температура кипения концентрированной серной кислоты составляет 338 градусов Цельсия.
Интересным фактом из курса химии является сокращение объема раствора. Примечательно то, что при смешении двух объемов серной кислоты и воды, соответственно, их итоговый объем будет меньше, чем суммарный.
Также обратите внимание на то, что удельный вес или плотность электролита авто или мото аккумулятора имеет непосредственную зависимость от тех температур, при которых работают аккумуляторы. Так, при эксплуатации в условиях низких температур нужен более плотный электролит. А в жарких странах – напротив – плотность электролита сознательно снижается. Это объясняется тем, что при таких температурах существенно повышается химическая активность раствора.
В заключение отметим, что плотность электролита также зависит от того, в каких режимах эксплуатируется батарея. Так, данный параметр для тяговых аккумуляторов обычно составляет 1.26 кг\с м³ , пусковые и осветительные источники питания имеют плотность до 1.3 кг\с м³ и т.д. Для автомобильных аккумуляторных батарей эта характеристика читается нормой, когда составляет 1.28 кг\с м³ .
23.08.2013, 69178 просмотров.
Какую кислоту заливают в аккумулятор
Большинство водителей никогда в жизни не задумывались, какую кислоту добавляют в аккумулятор авто и зачастую высказывают неправильные догадки. Одни скажут, что там вода, другие назовут соляную кислоту, поэтому мы расставим все точки над «и». В аккумуляторах применяется смесь серной кислоты и дист. воды. Знакомьтесь, это электролит.
На практике встречаются устройства, где в роли электролита выступает щелочь (никель-кадмиевые аккумуляторы). Также есть несколько гелевых устройств, но по факту гель – это та же самая кислота, находящаяся в другом состоянии или пропитывающий стекловолоконные частицы.
Она применяется в промышленном изготовлении АКБ для авто. Обычно, электролит — это 35% серной кислоты и 65% дист. воды. Заливать любую другую воду категорически запрещается, поскольку она содержит соли, которые существенно сократят срок работы АКБ.
Концентрированная серная кислота производится в 2 стадии. В первой её концентрацию доводят до 65-70%, а во второй – до 98%. Это необходимо для того, чтобы увеличить срок хранения кислоты. Вероятно даже повышение концентрации до 99%, но из-за потерь SO3 значение все равно будет снижено до 98 процентов.
Как сделать электролит в домашних условиях?
Рекомендуем купить его в магазине, но его можно сделать и своими руками.
Нам потребуются:
- Дистиллированная вода;
- Серная кислота;
- Емкость из стекла, керамики или свинца, устойчивая к кислотам;
- Эбонитовая палочка.
Чтобы сделать электролит надо залить воду в специальную емкость и добавить туда серную кислоту в пропорции 3:1. Тщательно перемешать смесь эбонитовой палочкой. Вещество плотно накрыть и оставить на 1 день до выпадения осадка.
Таблица для расчета приготовляемого электролитаНеобходимо сказать, что превышения в допустимой концентрации электролита может привести к самым неприятным последствиям. От чрезмерно концентрированного вещества пластины аккумулятора очень быстро «разъест», что в кратчайшие сроки вызовет выход аккумулятора из рабочего состояния.
В дист вода добавляем кислоту, а не наоборотА вот слишком низкий уровень плотности вещества может очень быстро вызывать сульфатацию. Наверняка вы знаете, что это такое. Нет? Это процесс оседания кристаллических осадков на пластинах, в результате чего аккумулятор теряет свои свойства и просто оказывается неспособным держать заряд долгое время.
Зачем нужен электролит?
Суть работы АКБ базируется на реакциях, проходящих только при помощи этого вещества. Батарея состоит из плюсовых и минусовых пластинок, погружаемых в кислотный раствор. Эти пластины оснащены токоотводными решетками, сделанными из свинца.
Как проконтролировать состояние электролита?
Держать под контролем состояние электролита нужно. Для контроля сгодится пластмассовый корпус от обычной пластиковой ручки. Открываем пробки и погружаем его к пластинам, после чего зажимаем сверху и вынуть. Идеальный уровень – 10-12 мм. Если надо, дольем электролит.
Измерение уровня электролита в АКБОчень важно следить за временем года и параметрами раствора в соответствии с ним. Можно существенно продлить жизнь батареи, если использовать растворы с разными параметрами в разное время. К примеру, слишком концентрированное вещество в летнее время деструктивно воздействует на АКБ. Высокая плотность увеличивает энергопотери, а серный ангидрид может полностью разрушить электроды устройства.
Срок эксплуатации электролита
У такого электролита нет срока эксплуатации. Данный критерий может быть определен только по способности выполнения своих функций на 100%. Среди факторов, которые могут повлиять на жизненный цикл электролита, важнейшими являются:
- Плотность;
- Температуру работы аккумулятора;
- Заряд.
Если все показатели в норме, то и электролит не будет тревожить Вас годами.
Как увеличить плотность вещества?
Увеличить плотность можно при повышении температуры и гидролиза. Также важно постоянно добавлять дистиллят для поддержания показателей на нормальном уровне. Если же концентрация кислоты ниже 1,275 грамм на сантиметр кубический, её нужно поднять.
Корректировка плотности электролита в АКБПовысить такой уровень можно 2-мя способами: сменой содержимого или доливом концентрированной кислоты.
Если разбавлять жидкость, то необходимо совершить определенные действия для всех банок:
- Откачать максимум электролита при помощи шприца;
- Внести в банку половину от его объема;
- Подать нагрузку с низкой мощностью для смешивания жидкости.
- Если изменений в уровне нет, добавляем во вторую половину электролит и получаем идеальную плотность.
Кислота – вредная субстанция для кожи. Использование резиновых перчаток, фартука и защитных очков при работе с этим веществом категорически обязательно!
Как заливать и доливать кислоту?
Электролит заливается при помощи трубки до 15 мм над пластинками батареи. Затем оставляем аккумулятор на 2 часа для остывания и заряжаем током в 10 раз меньшим от объема АКБ.
Ключевые характеристики надо проверять пару раз в году с помощью особого прибора и не пропускать проверки.
При смешивании дистводы с кислотой, важно добавлять именно кислоту в воду, так как в обратном случае есть вероятность активации бурной реакции вещества с тепловыделением, доведением её до состояния кипения.
Внимательно соблюдайте все вышеперечисленные рекомендации и АКБ будет служить очень долгое время!
Сдать старый АКБ за деньги вы сможете в нашей фирме, тарифы на приём акумуляторов на этой странице.
профессионал — Инструкция по нейтрализации отработанной серной кислоты аккумуляторных батарей (2 класса опасности)
1.Общие требования безопасности.
При сборе, хранении, нейтрализации отработанной серной кислоты от аккумуляторных батарей следует учитывать особенности ее эксплуатации и степень опасности.
Природные воды имеют нейтральную, слабокислую или слабощелочную реакцию, рН их находится в пределах 6.5 — 8,5. Электролит имеет кислую рН среду и представляет собой серную кислоту плотностью 1,2 — 1,27. Аккумуляторная серная кислота является достаточно концентрированной и не подлежит утилизации без предварительной нейтрализации.
Растворы серной кислоты оказывают вредное воздействие на организм человека.
При нагревании серной кислоты образуются пары сернистого ангидрида, которые, соединяясь с парами воздуха, образуют кислотный туман. При вдыхании паров серной кислоты раздражаются и прижигаются слизистые оболочки верхних дыхательных путей.
При попадании на кожу серная кислота вызывает сильные ожоги, болезненные и трудно поддающиеся лечению. Попадание серной кислоты в глаза грозит потерей зрения.
Персонал, занятый нейтрализацией аккумуляторной серной кислоты, должен работать в одежде из кисло-защитной ткани, прорезиненных фартуках, резиновых сапогах, резиновых кислостойких перчатках, защитных очках или щитках из оргстекла, иметь фильтрующий противогаз марки В.
Места сбора и нейтрализации аккумуляторной серной кислоты должны иметь предупредительные надписи.
2. Требования безопасности перед началом работы.
Получить инструктаж от ответственного за нейтрализацию, о мерах безопасности и производственной санитарии при работе с аккумуляторной серной кислотой.
Подготовить и проверить исправность защитных средств, приспособлений и другого инвентаря. Следует иметь в виду, что любые разбавленные растворы серной кислоты, к которым относится и электролит, крайне • агрессивны. Вследствие этого нейтрализацию электролита необходимо проводить с максимально возможной быстротой и без перерывов.
3.Требования безопасности во время работы.
Нейтрализацию отработанного электролита проводят известковым молоком. Для приготовления одного литра известкового молока необходимо взять 100 граммов не гашенной извести (СаО). Процесс гашения извести сопровождается сильным разогревом и разбрызгиванием.
Для нейтрализации 1 литра электролита необходимо взять 7 литров известкового молока, при этом электролит порциями добавляют в известковое молоко. Окончание нейтрализации проверяют с помощью раствора индикатора (метилоранжа), цвет которого в нейтральном растворе -желтый, в кислом — красный.
Процесс нейтрализации электролита известковым молоком проходит с выделением теплоты и образованием нерастворимого в воде соединения сульфата кальция. Осветление воды после нейтрализации длится 2-3 часа. Осветленная вода сливается в ливневую канализацию. Шлам отработанного электролита и образовавшийся в процессе нейтрализации электролита и образовавшийся в процессе нейтрализации сульфат кальция, необходимо просушить, после чего сложить в место сбора отходов. По окончании работы необходимо провести уборку рабочего места, все приспособления, инструменты и материалы сложить в указанное место.
В случае проливов серной кислоты на пол ее следует немедленно нейтрализовать, посыпать известью, убрать лопатой, а затем тщательно промыть это место сильной струей воды. При попадании кислоты на одежду ее необходимо смыть обильной струей воды, нейтрализовать 2-3% раствором соды и снова промыть водой. При необходимости сдать спецодежду на санобработку и принять душ.
4. Оказание первой медицинской помощи.
Рабочим, участвующим в нейтрализации отработанного электролита, необходимо знать методы оказания первой помощи при несчастных случаях.
При ожогах кожи кислотой разрезать и осторожно удалить клочки одежды. Обработать кожу водой. Несильной струей воды попытаться удалить остатки электролита. После промывания водой наложить примочку с раствором пищевой соды.
| _______________________ | ______________________ |
|
Должность лица, ответственного за охрану окружающей среды |
ФИО |
Скачать инструкцию бесплатно в формате pdf
Свинцово-кислотные батареи Учебное пособие по химии
Пожалуйста, не блокируйте рекламу на этом сайте.
Без рекламы = для нас нет денег = для вас нет бесплатных вещей!
Свинцово-кислотный гальванический элемент, вырабатывающий электричество (разряд)
Разряд свинцово-кислотного элемента:
- — спонтанная окислительно-восстановительная реакция (E (окислительно-восстановительный) положительный)
- преобразует химическую энергию, хранящуюся в свинце, диоксиде свинца и серной кислоте, в электрическую энергию.
Ниже приведена схема свинцово-кислотного элемента во время разряда:
анод (-) катод (+) и — → электролит |
На аноде во время разряда:
- Электрод: губчатый свинец, Pb (s) в корпусе для выводов (пористая свинцовая пластина)
Окисление происходит на аноде.
- Свинец на аноде окислен:
Pb (т) → Pb 2+ (водн.) + 2e —
- Pb 2+ реагирует с SO 4 2- в серной кислоте с образованием PbSO 4 (s) в виде осадка:
Pb 2+ (водн.) + SO 4 2- (водн.) → PbSO 4 (с)
PbSO 4 (s) прилипает к выводной рамке анода.
- Общая реакция на аноде равна
Pb (с) + SO 4 2- (водн.) → PbSO 4 (с) + 2e —
- Электронов на аноде.
- Анод отрицательный.
- Электроны перемещаются от анода (-) к катоду (+) по проводам, соединяющим электроды.
На катоде во время разряда:
- Электрод: свинцовая рамка, покрытая диоксидом свинца, PbO 2 (т)
- Восстановление происходит на катоде.
- Свинец в диоксиде свинца восстанавливается на катоде протонами серной кислоты:
PbO 2 (с) + 4H + (водн.) + 2e — → Pb 2+ (водн.) + 2H 2 O (л)
- Pb 2+ реагирует с SO 4 2- в серной кислоте с образованием PbSO 4 (s) в виде осадка:
Pb 2+ (водн.) + SO 4 2- (водн.) → PbSO 4 (с)
PbSO 4 (s) прилипает к выводной рамке катода.
- Общая реакция на катоде равна
PbO 2 (с) + 4H + (водн.) + 2e — + SO 4 2- (водн.) → PbSO 4 (с) + 2H 2 O (л)
- Электроны расходуются на катоде.
- Катод положительный.
- Протоны, H + (водн.) , расходуются на катоде.
Вен может использовать реакцию окисления на аноде и реакцию восстановления, которая происходит на катоде, чтобы написать общее окислительно-восстановительное уравнение для свинцово-кислотного элемента:
| анод реакция: | Pb (т.) + SO 4 2- (водн.) | → | ПбСО 4 (с) + | |
|---|---|---|---|---|
| катод реакция: | PbO 2 (с) + 4H + (водн.) + SO 4 2- (водн.) + | → | PbSO 4 (с) + 2H 2 O (л) | |
| всего реакция: | Pb (с) + PbO 2 (с) + 4H + (водн.) + 2SO 4 2- (водн.) | → | 2PbSO 4 (с) + 2H 2 O (л) | E & прибл; +2 В |
По мере разряда свинцово-кислотного элемента:
- PbSO 4 осаждается и откладывается как на аноде, так и на катоде.
- H + из электролита (H 2 SO 4 (водн.) ) используется для получения воды на катоде.
- Концентрация H + со временем будет уменьшаться (концентрация H 2 SO (водн.) уменьшается).
- pH электролита (H 2 SO 4 (водн.) ) увеличится.
Последовательное соединение свинцово-кислотных гальванических элементов для изготовления свинцово-кислотных аккумуляторов позволяет нам изготавливать аккумуляторы с напряжением более 2 В:
| количество ячеек в серии | 2 | 3 | 4 | 5 | 6 |
|---|---|---|---|---|---|
| примерное напряжение | 2 × 2 = 4 В | 3 × 2 = 6 В | 4 × 2 = 8 В | 5 × 2 = 10 В | 6 × 2 = 12 В |
Зарядка свинцово-кислотного гальванического элемента
Зарядка свинцово-кислотного аккумулятора:
- — это неспонтанная окислительно-восстановительная реакция (E (окислительно-восстановительный) отрицательная), то есть электролитический процесс.
- требует ввода чуть более 2 вольт на ячейку для запуска спонтанных реакций в обратном направлении.
- преобразует электрическую энергию обратно в химическую энергию, которая хранится в свинце, диоксиде свинца и серной кислоте в элементе.
На схеме ниже показан свинцово-кислотный аккумулятор во время перезарядки:
катод (-) анод (+) ← e — электролит |
На катоде во время перезарядки:
На аноде во время перезарядки:
Используя полууравнения для реакций, происходящих на аноде и катоде, мы можем записать общую окислительно-восстановительную реакцию для свинцово-кислотного элемента во время перезарядки:
| катод реакция: | ПбСО 4 (с) + | → | Pb (т.) + SO 4 2- (водн.) | |
|---|---|---|---|---|
| анод реакция: | PbSO 4 (с) + 2H 2 O (л) | → | PbO 2 (с) + 4H + (водн.) + SO 4 2- (водн.) + | |
| всего реакция: | 2PbSO 4 (с) + 2H 2 O (л) | → | Pb (с) + PbO 2 (с) + 4H + (водн.) + 2SO 4 2- (водн.) | E & прибл; -2 В |
По мере перезарядки свинцово-кислотного элемента:
- PbSO 4 (s) на каждом электроде удаляется.
- Концентрация H + увеличивается.
- pH электролита (H 2 SO 4 (водн.) ) снижается.
Для зарядки свинцово-кислотного аккумулятора требуется минимум 2 В на элемент:
| количество ячеек в серии | 2 | 3 | 4 | 5 | 6 |
|---|---|---|---|---|---|
| Требуемое напряжение перезарядки | > 4 В | > 6 В | > 8 В | > 10 В | > 12 В |
При перезарядке батареи происходит электролиз воды с образованием газообразного водорода и газообразного кислорода.
Пузырьки газа разрушают поверхность электродов, вызывая падение PbSO 4 (s) с электродов.
Это уменьшает емкость ячейки.
Работа свинцово-кислотных аккумуляторов
Свинцово-кислотные аккумуляторы состоят из отрицательного электрода, сделанного из губчатого или пористого свинца. Свинец пористый, что способствует образованию и растворению свинца. Положительный электрод состоит из оксида свинца.Оба электрода погружены в электролитический раствор серной кислоты и воды. В случае, если электроды входят в контакт друг с другом в результате физического движения батареи или изменения толщины электродов, два электрода разделяет электрически изолирующая, но химически проницаемая мембрана. Эта мембрана также предотвращает короткое замыкание через электролит. Свинцово-кислотные батареи накапливают энергию за счет обратимой химической реакции, показанной ниже.
Общая химическая реакция:
PbO2 + Pb + 2h3SO4⇔заряженный разряд2PbSO4 + 2h3O
На минусовой клемме реакции заряда и разряда:
Pb + SO42-заряженныйразрядPbSO4 + 2e-
На положительном выводе реакции заряда и разряда:
PbO2 + SO42- + 4H ++ 2e-заряженный разрядPbSO4 + 2h3O
Как показывают приведенные выше уравнения, разрядка батареи вызывает образование кристаллов сульфата свинца как на отрицательной, так и на положительной клеммах, а также высвобождение электронов из-за изменения валентного заряда свинца.Для образования этого сульфата свинца используется сульфат сернокислотного электролита, окружающего аккумулятор. В результате электролит становится менее концентрированным. Полный разряд приведет к тому, что оба электрода будут покрыты сульфатом свинца и водой, а не серной кислотой, окружающей электроды. При полном разряде два электрода сделаны из одного материала, и между ними нет химического потенциала или напряжения. На практике, однако, разряд прекращается при напряжении отсечки, задолго до этого момента.Следовательно, аккумулятор не должен разряжаться ниже этого напряжения.
Между полностью разряженным и заряженным состояниями свинцово-кислотная батарея будет испытывать постепенное снижение напряжения. Уровень напряжения обычно используется для обозначения степени заряда аккумулятора. Зависимость аккумулятора от уровня заряда показана на рисунке ниже. Если аккумулятор оставить на низком уровне заряда в течение длительного периода времени, могут вырасти крупные кристаллы сульфата свинца, что необратимо снижает емкость аккумулятора.Эти более крупные кристаллы не похожи на типичную пористую структуру свинцового электрода, и их трудно превратить обратно в свинец.
Напряжение свинцово-кислотного аккумулятора при зарядке.
В результате реакции зарядки сульфат свинца на отрицательном электроде превращается в свинец. На положительном конце реакция превращает свинец в оксид свинца. В качестве побочного продукта этой реакции выделяется водород. Во время первой части цикла зарядки преобладающей реакцией является превращение сульфата свинца в свинец и оксид свинца.Однако по мере того, как происходит зарядка и большая часть сульфата свинца превращается либо в свинец, либо в диоксид свинца, зарядный ток электролизует воду из электролита, и выделяются водород и газообразный кислород, процесс, известный как «выделение газа» из батареи. Если ток подается в батарею быстрее, чем может быть преобразован сульфат свинца, то выделение газа начинается до того, как весь сульфат свинца преобразуется, то есть до того, как батарея полностью зарядится. Газообразование создает несколько проблем в свинцово-кислотной батарее.Газовыделение батареи не только вызывает проблемы безопасности из-за взрывоопасной природы производимого водорода, но также снижает количество воды в батарее, которую необходимо заменять вручную, вводя в систему компонент для обслуживания. Кроме того, выделение газа может вызвать отделение активного материала от электролита, что приведет к необратимому снижению емкости аккумулятора. По этим причинам аккумулятор не следует регулярно заряжать выше напряжения, которое вызывает газообразование. Напряжение газовыделения изменяется в зависимости от скорости заряда.
Сульфат свинца является изолятором, и поэтому способ образования сульфата свинца на электродах определяет, насколько легко можно разрядить аккумулятор.
Свинцовая аккумуляторная батарея| Введение в химию
Цель обучения
- Вспомните химическую реакцию, которая происходит в свинцовых аккумуляторных батареях
Ключевые моменты
- Свинцово-кислотные батареи, также известные как свинцовые аккумуляторные батареи, могут накапливать большой заряд и обеспечивать высокий ток в течение коротких периодов времени.
- Базовая конструкция свинцово-кислотных аккумуляторов не претерпела значительных изменений с 1859 года, когда их спроектировал Планте, хотя некоторые улучшения были внесены Фор.
- Свинцово-кислотные аккумуляторы можно заряжать, что важно при их использовании в автомобилях.
- Разрядка накопленной энергии зависит от того, как положительная, так и отрицательная пластины превращаются в сульфат свинца (II), а электролит теряет большую часть растворенной серной кислоты.
Срок
- лигносульфонат Водорастворимые анионные полиэлектролитные полимеры; они являются побочными продуктами производства древесной массы с использованием сульфитной варки.
Свинцовые батареи
Свинцовая аккумуляторная батарея, также известная как свинцово-кислотная батарея, является самым старым типом аккумуляторных батарей и одним из наиболее распространенных устройств хранения энергии. Эти батареи были изобретены в 1859 году французским физиком Гастоном Планте, и они до сих пор используются во множестве приложений. Большинство людей привыкло использовать их в транспортных средствах, где они могут обеспечивать высокие токи для запуска двигателя.
Хотя батареи надежны, у них ограниченный срок службы, они тяжелы при транспортировке и содержат токсичные материалы, которые требуют специальных методов удаления по окончании срока службы.Свинцово-кислотные батареи имеют умеренную удельную мощность и хорошее время отклика. В зависимости от используемой технологии преобразования энергии батареи могут перейти от приема энергии к мгновенной подаче энергии. Свинцово-кислотные аккумуляторы подвержены влиянию температуры и должны поддерживаться в надлежащем состоянии для достижения максимального срока службы.
Разработка свинцовой батареи
В конструкции свинцово-кислотного элемента Планте положительная и отрицательная пластины были сделаны из двух спиралей свинцовой фольги, разделенных листом ткани и скрученных.Ячейки изначально были малой вместимостью. Требовался медленный процесс «формовки» для коррозии свинцовой фольги, образования диоксида свинца на пластинах и придания им шероховатости для увеличения площади поверхности. Пластины Планте все еще используются в некоторых стационарных приложениях, где на пластинах имеются механические канавки для увеличения площади поверхности.
Свинцовая аккумуляторная батарея Схема, показывающая, как свинцовая аккумуляторная батарея состоит из шести двухвольтовых элементов, соединенных последовательно. Также показан состав каждой ячейки.Конструкция из клееных пластин Камиллы Альфонса Фор типична для современных автомобильных аккумуляторов.Каждая пластина состоит из прямоугольной свинцовой сетки. Отверстия решетки заполнены пастой из красного свинца и 33-процентной разбавленной серной кислоты. Эта пористая паста позволяет кислоте реагировать со свинцом внутри пластины, что увеличивает площадь поверхности. После высыхания пластины складываются с помощью подходящих разделителей и вставляются в аккумуляторный контейнер. Обычно используется нечетное количество пластин, с отрицательной пластиной на одну больше, чем положительной. Каждая альтернативная пластина подключается.
Паста содержит технический углерод, сульфат бария и лигносульфонат.Сульфат бария действует как затравочный кристалл для реакции сульфата свинца в свинец. Лигносульфонат предотвращает образование твердой массы отрицательной пластиной во время цикла разряда, а вместо этого позволяет формировать длинные игольчатые кристаллы. Технический углерод противодействует эффекту ингибирования образования, вызванному лигносульфонатами.
Разрядная химия
В разряженном состоянии как положительная, так и отрицательная пластины становятся сульфатом свинца (II) (PbSO 4 ). Электролит теряет большую часть растворенной серной кислоты и превращается в основном в воду.Процесс разряда управляется проводимостью электронов от отрицательной пластины обратно в ячейку на положительной пластине во внешней цепи.
Отрицательная реакция пластины: Pb (s) + HSO 4 — (водн.) → PbSO 4 (s) + H + (водн.) + 2e —
Положительная реакция пластины: PbO 2 (с) + HSO 4 — (водн.) + 3H + (водн.) + 2e — → PbSO 4 (с) + 2H 2 O (л)
Комбинируя эти две реакции, можно определить общую реакцию:
Pb (с) + PbO 2 (с) + 2H + (вод.) + 2HSO 4 — (вод.) → 2PbSO 4 (с) + 2H 2 O (л)
Зарядная химия
Аккумулятор этого типа можно заряжать.В заряженном состоянии каждая ячейка содержит отрицательные пластины из элементарного свинца (Pb) и положительные пластины из оксида свинца (IV) (PbO 2 ) в электролите примерно 4,2 М серной кислоты (H 2 SO 4 ). . Процесс зарядки осуществляется за счет принудительного удаления электронов с положительной пластины и принудительного введения их в отрицательную пластину источником заряда.
Отрицательная реакция пластины: PbSO 4 (с) + H + (вод.) + 2e — → Pb (с) + HSO 4 — (вод.)
Положительная реакция пластины: PbSO 4 (с) + 2H 2 O (л) → PbO 2 (с) + HSO 4 — (водн.) + 3H + (водн.) + 2e –
Объединение этих двух реакций дает полную реакцию, обратную реакции разряда:
2PbSO 4 (с) + 2H 2 O (л) → Pb (с) + PbO 2 (с) + 2H + (водн.) + 2HSO 4 — (водн.)
Обратите внимание, что реакция зарядки прямо противоположна реакции разряда.
Показать источникиBoundless проверяет и курирует высококачественный контент с открытой лицензией из Интернета. Этот конкретный ресурс использовал следующие источники:
Что такое аккумуляторная кислота?
Аккумуляторная кислота обычно относится к кислоте, используемой в свинцово-кислотных аккумуляторах, хотя она необходима для функционирования любой кислотной аккумуляторной батареи или химического элемента. Хранение химической энергии для возможного использования в электричестве — это основной принцип, лежащий в основе батарей, в том числе для батарей, использующих кислоту.
Принцип действия этого электрохимического процесса во многом обусловлен особой структурой и химическим составом этих устройств, но аккумуляторная кислота также играет решающую роль.
Связанный: Купить аккумуляторную кислоту онлайн Из чего состоит аккумуляторная кислота?Обычно относится к типу кислоты, используемой в перезаряжаемых свинцово-кислотных аккумуляторах, например, используемых в автомобилях, аккумуляторная кислота состоит из серной кислоты (H 2 SO 4 ), которая была разбавлена очищенной водой до концентрации около 30-50%.В этом контексте кислотный pH аккумуляторной кислоты составляет 0,8. Вот почему с ним нужно обращаться осторожно.
Свинцово-кислотные батареи состоят из двух проводящих свинцовых пластин, называемых электродами, которые заполнены вязким гелеобразным веществом. Между этими пластинами находится разбавленный раствор серной кислоты, также известный как электролит. Другой ключевой частью свинцово-кислотных аккумуляторов является разделитель, который служит изолятором, предотвращая прямое соприкосновение двух пластин друг с другом, что может привести к короткому замыканию.
Аккумуляторная кислота — это серная кислота, разбавленная очищенной водой. Что делает аккумуляторная кислота?Проще говоря, аккумуляторная кислота способствует преобразованию накопленной химической энергии в электрическую. Обычная батарея обычно состоит из трех основных частей:
- Отрицательный электрод , также известный как анод , который отправляет электроны во внешнюю цепь. Обычно это делается из губчатого свинца
- Положительный электрод или катод , который принимает электроны от внешней цепи.Обычно это диоксид свинца
- Электролит , обеспечивающий ионную проводимость . Обычно это жидкий раствор растворителя и растворенных солей
Электрохимическая реакция, обеспечиваемая кислотой аккумулятора, позволяет стабильному току проходить через пары электродов, когда электричество входит в анод и выходит из катода.
Когда батарея разряжается или используется в качестве источника питания, серная кислота в электролите реорганизует свои ионы так, чтобы они были менее концентрированными и более похожими на H 2 O.При этом выделяется серия сульфатов, которые покрывают свинцовые пластины анода и катода. Это уменьшает область, в которой могут происходить дальнейшие электрохимические реакции. Эта площадь поверхности, постоянно выделяя ионы, будет становиться все меньше и меньше по мере использования большего количества ионов.
Батарея будет продолжать работать до тех пор, пока не перестанет обеспечивать достаточную мощность из-за того, что ее электролит обеднен сульфат-ионами. Чтобы снова заработать, аккумулятор необходимо перезарядить — процесс, который, по сути, является обратной реакцией того, что мы только что описали.
В двух словах, зарядка аккумулятора преобразует электрическую энергию в химическую энергию, а при использовании (или разрядке) аккумулятора используется накопленная химическая энергия, преобразовывая ее в электрическую энергию.
Почему батареи содержат кислоту?Батареи содержат кислоту, поскольку она играет ключевую роль в протекающей электрохимической реакции. Также называемый аккумуляторным электролитом, аккумуляторная кислота — это среда, которая переносит электрический ток между положительным и отрицательным электродами.
Однако, хотя для облегчения реакции аккумуляторным батареям необходим электролит, это не обязательно должен быть разбавленный раствор серной кислоты. Электролиты в батареях могут быть растворителями, смешанными с растворенными кислотами или щелочами, а типичные батареи AA / AAA / D даже содержат твердые, а не жидкие электролиты.
Насколько сильна кислота в аккумуляторе?Аккумуляторная кислота обычно имеет концентрацию около 15–35%, хотя ее крепость может достигать 50%.Любая концентрация серной кислоты в свинцово-кислотных аккумуляторах вызывает сильную коррозию. Неправильное обращение с этим химическим веществом может привести к необратимой слепоте, тяжелым ожогам, повреждению внутренних органов при проглатывании или даже смерти.
Аккумуляторная кислота также легко воспламеняется и может воспламениться под воздействием высокой температуры или давления. Наряду с этими особенностями стоит отметить уникальную химическую структуру аккумуляторной кислоты и то, как она вступает в реакцию с другими материалами, создавая электричество или накапливая химическую энергию.
Какова формула аккумуляторной кислоты?Аккумуляторная кислота не имеет определенной формулы, но обычно она состоит только из серной кислоты (H 2 SO 4 ) и воды (H 2 O) с приблизительным уровнем pH 0.8 при концентрации 4-5 моль / л.
Как работает батарея, электроны текут от отрицательно заряженной свинцовой пластины к положительно заряженной пластине из диоксида свинца. Это движение электронов заставляет сульфаты, высвобождаемые из аккумуляторной батареи, покрывать анод кислотой, которая высвобождает избыточные электроны в устройство и обратно на катод, тем самым облегчая электрический поток. Формула этой реакции:
Pb (с) + PbO 2 (с) + 2 H 2 SO 4 (водн.) → 2PbSO 4 (с) + 2H 2 O
Аккумуляторная кислота содержится в свинцово-кислотных аккумуляторах, которые обычно используются для питания отстойников в случае аварийного освещения. Что происходит при использовании батареи?Что на самом деле происходит, когда батарея используется, так это то, что отрицательно заряженные сульфат-ионы в кислоте батареи попадают на отрицательный электрод, т.е.е. анод. Здесь они высвобождают свой отрицательный заряд, в то время как остальные ионы сульфата соединяются с электродом с образованием сульфата свинца. Этот процесс сменяется высвобождением избыточных электронов, выходящих из отрицательного электрода и обратно к положительному электроду, то есть катоду.
Это, однако, со временем снижает концентрацию электролита, так как в растворе кислоты образуется больше сульфата свинца и больше воды. Это происходит, когда водород отделяется от H 2 SO 4 и вступает в реакцию с диоксидом свинца на катоде, что увеличивает концентрацию воды, поскольку больше ионов SO 4 будет использоваться для покрытия электрода во время использования батареи. .Это будет происходить до тех пор, пока аккумуляторная кислота не станет все более и более разбавленной, что сделает ее менее способной к дальнейшим электрохимическим реакциям из-за недостатка ионов сульфата.
По сути, постоянное движение ионов — это то, что создает стабильный ток в батареях. Когда кислород в пластине диоксида свинца реагирует с ионами водорода с образованием воды, а отделенный сульфат реагирует с другой пластиной с образованием большего количества сульфата свинца, остается более разбавленный раствор серной кислоты, который можно перезарядить путем реверсирования процесса. я.е. подавая в него электричество и преобразовывая его в накопленную химическую энергию.
Эти электрохимические реакции в батареях были бы невозможны без аккумуляторной кислоты. Однако по мере развития технологий появляются разные типы аккумуляторов, и необходимо пересмотреть технические аспекты работы обычных автомобильных аккумуляторов, чтобы позволить новаторам создавать больше функций для аккумуляторов, с кислотой или без нее.
Что такое аккумуляторная кислота?
Аккумуляторная кислота может относиться к любой кислоте, используемой в химическом элементе или аккумуляторе, но обычно этот термин описывает кислоту, используемую в свинцово-кислотных аккумуляторах, например, в автомобилях.
Кислота для автомобилей или автомобильных аккумуляторов — это 30-50% серная кислота (H 2 SO 4 ) в воде. Обычно кислота имеет мольную долю серной кислоты 29–32%, плотность 1,25–1,28 кг / л и концентрацию 4,2–5 моль / л. Аккумуляторная кислота имеет pH примерно 0,8.
Строительство и химическая реакция
Свинцово-кислотная батарея состоит из двух свинцовых пластин, разделенных жидкостью или гелем, содержащим серную кислоту в воде. Аккумуляторная батарея заряжается и разряжается химическими реакциями.Когда батарея используется (разряжена), электроны перемещаются от отрицательно заряженной свинцовой пластины к положительно заряженной.
Отрицательная реакция пластины:
Pb (s) + HSO 4 — (водн.) → PbSO 4 (s) + H + (водн.) + 2 e —
Положительная реакция пластины:
PbO 2 (с) + HSO 4 — + 3H + (водн.) + 2 e — → PbSO 4 (с) + 2 H 2 O (л)
Что можно объединить, чтобы записать общую химическую реакцию:
Pb (с) + PbO 2 (с) + 2 H 2 SO 4 (водн.) → 2 PbSO 4 (с) + 2 H 2 O (л)
Зарядка и разрядка
Когда аккумулятор полностью заряжен, отрицательная пластина — это свинец, электролит — концентрированная серная кислота, а положительная пластина — диоксид свинца.Если аккумулятор чрезмерно заряжен, при электролизе воды образуется газообразный водород и газообразный кислород, которые теряются. Некоторые типы батарей позволяют добавлять воду, чтобы восполнить потерю.
Когда аккумулятор разряжен, обратная реакция образует сульфат свинца на обеих пластинах. Если аккумулятор полностью разряжен, в результате образуются две идентичные пластины сульфата свинца, разделенные водой. На этом этапе аккумулятор считается полностью разряженным и не может восстановиться или снова зарядиться.
Свинцовая аккумуляторная батареяI
Вспомогательная батарея: Свинцовая аккумуляторная батареяT Электроды элементов свинцовой аккумуляторной батареи состоят из свинцовых решеток.Отверстия анодной сетки заполнены губчатым (пористым) свинцом. Отверстия катодной сетки заполнены диоксидом свинца { PbO 2 }. Разбавленная серная кислота { H 2 SO 4 } служит электролитом. Когда аккумулятор подает ток, то есть разряжает , провод на анод окисленный:
Pb Pb 2+ + 2 e —
B , потому что ионы свинца находятся в присутствии водного сульфат-ионы (из серной кислоты), осадки нерастворимого сульфата свинца на электрод.Общая реакция на аноде составляет следовательно:
Пб + СО 4 2– PbSO 4 (электрод) + 2 e —
E Лектроны, истекающие из анода, одновременно уменьшают диоксид свинца на катоде :
2 e — + PbO 2 + 4 H + Pb 2+ + 2 H 2 O
A , образующиеся ионы свинца реагируют с водными сульфат-ионами с образованием нерастворимого сульфата свинца на электроде, и общая реакция на катоде составляет:
2 e — + PbO 2 + 4 H + + SO 4 2– PbSO 4 (электрод) + 2 H 2 O
Что каково общее уравнение для свинцовой аккумуляторной батареи при ее разряде?
Напишите свой ответ на листе бумаги.Когда закончите, нажмите на зеленый проверяет ответы на каждый шаг.
T Свинцовая ячейка хранения может быть перезаряжена , пропуская ток в обратном направлении. Половина реакции полностью противоположны тем, которые происходят, когда элемент работает как гальванический элемент.
| Примечание: важным аспектом свинцового накопителя является то, что продукты реакций на аноде и катоде нерастворимы (в каждом случае сульфат свинца).Это означает, что эти вещества легко доступны для участия в обратных реакциях, перезаряжающих клетку! |
Свинцово-кислотный аккумулятор: работа, конструкция и зарядка / разрядка
Практически каждое портативное устройство состоит из аккумулятора. Батарея — это накопительное устройство, в котором накапливается энергия для обеспечения ее в любой момент. В современном мире электроники доступны различные типы батарей, среди которых Свинцовые Кислотные батареи обычно используются для источников питания высокой мощности.Обычно свинцово-кислотные батареи больше по размеру, имеют прочную и тяжелую конструкцию, они могут хранить большое количество энергии и обычно используются в автомобилях и инверторах.
Даже после конкуренции с литий-ионными батареями спрос на свинцово-кислотные батареи растет день ото дня, потому что они дешевле и проще в обращении по сравнению с литий-ионными батареями. Согласно некоторым исследованиям рынка, рынок свинцово-кислотных аккумуляторов в Индии будет расти со среднегодовым темпом роста более 9% в течение 2018-24 годов. Таким образом, он пользуется огромным рыночным спросом в автоматизации, автомобилестроении и бытовой электронике.Хотя большая часть электромобилей поставляется с литий-ионными батареями, все же есть много электрических двухколесных транспортных средств, которые используют свинцово-кислотные батареи для питания транспортного средства.
В предыдущем уроке мы узнали о литий-ионных аккумуляторах, здесь мы разберемся в работе , конструкции и применении свинцово-кислотных аккумуляторов. Мы также узнаем о характеристиках зарядки / разрядки, требованиях и безопасности свинцово-кислотных аккумуляторов.
Конструкция свинцово-кислотной батареиЧто такое свинцово-кислотный аккумулятор? Если мы сломаем название Свинцово-кислотная батарея, мы получим Свинец, Кислота и Батарея .Свинец — это химический элемент (обозначение — Pb, атомный номер 82). Это мягкий и податливый элемент. Мы знаем, что такое кислота; он может отдавать протон или принимать пару электронов, когда реагирует. Итак, аккумулятор, который состоит из свинца и безводной свинцовой кислоты (иногда ошибочно называемой пероксидом свинца), называется свинцово-кислотным аккумулятором.
Итак, какова внутренняя конструкция?
Свинцово-кислотная батарея состоит из следующих элементов, мы можем видеть это на изображении ниже:
Свинцово-кислотная батарея состоит из пластин , сепаратора и электролита, твердого пластика с твердым резиновым корпусом .
В аккумуляторах пластины двух типов , положительные и отрицательные. Положительный состоит из диоксида свинца, а отрицательный — из губчатого свинца. Эти две пластины разделены разделителем , который представляет собой изоляционный материал. Вся конструкция хранится в твердом пластиковом корпусе с электролитом. Электролит — вода и серная кислота.
Жесткий пластиковый корпус одноклеточный. Одно хранилище ячеек обычно 2.1В. По этой причине свинцово-кислотная батарея на 12 В состоит из 6 ячеек и обычно обеспечивает 6 x 2,1 В / элемент = 12,6 В.
Теперь, какова емкость накопителя заряда?
Это сильно зависит от активного материала (количества электролита) и размера пластины. Возможно, вы видели, что емкость литиевой батареи описывается в мАч или миллиампер-часах, но в случае свинцово-кислотной батареи это ампер-час . Мы опишем это в следующем разделе.
Работа свинцово-кислотной батареиРабота свинцово-кислотного аккумулятора — это все о химии, и очень интересно узнать о ней. В процессе зарядки и разрядки свинцово-кислотных аккумуляторов происходят огромные химические процессы. При растворении кислоты молекулы разбавленной серной кислоты H 2 SO 4 распадаются на две части. Он создаст положительные ионы 2H + и отрицательные ионы SO 4 -. Как мы уже говорили ранее, два электрода соединены как пластины, анод и катод.Анод улавливает отрицательные ионы, а катод притягивает положительные ионы. Эта связь в аноде и SO 4 — и катоде с 2H + обменивается электронами и далее реагирует с h3O или с водой (разбавленная серная кислота, серная кислота + вода).
Батарея имеет два состояния химической реакции: Зарядка и Разрядка .
Свинцово-кислотный аккумулятор ЗарядкаКак мы знаем, для зарядки аккумулятора нам необходимо обеспечить напряжение, превышающее напряжение на клеммах.Таким образом, для зарядки аккумулятора 12,6 В можно подать напряжение 13 В.
Но что на самом деле происходит, когда мы заряжаем свинцово-кислотную батарею?
Ну, те же химические реакции, которые мы описали ранее. В частности, когда аккумулятор соединен с зарядным устройством, молекулы серной кислоты распадаются на два иона: положительные ионы 2H + и отрицательные ионы SO 4 -. Водород обменивается электронами с катодом и становится водородом, этот водород реагирует с PbSO 4 на катоде и образует серную кислоту (H 2 SO 4 ) и свинец (Pb).С другой стороны, SO 4 — обмениваются электронами с анодом и превращаются в радикал SO 4 . Этот SO 4 реагирует с PbSO 4 анода и образует пероксид свинца PbO 2 и серную кислоту (H 2 SO 4 ). Энергия накапливается за счет увеличения плотности серной кислоты и увеличения потенциального напряжения ячейки.
Как объяснено выше, в процессе зарядки на аноде и катоде происходят следующие химические реакции.
На катоде
PbSO 4 + 2e - => Pb + SO 4 2-
На аноде
PbSO 4 + 2H 2 O => PbO 2 + SO 4 2- + 4H - + 2e -
В сочетании двух приведенных выше уравнений общая химическая реакция будет
.2PbSO 4 + 2H 2 O => PbO 2 + Pb + 2H 2 SO 4
Существуют различные методы зарядки свинцово-кислотных аккумуляторов.Каждый метод можно использовать для определенных свинцово-кислотных аккумуляторов для конкретных приложений. В некоторых приложениях используется метод зарядки с постоянным напряжением , в некоторых приложениях используется метод с постоянным током , в то время как зарядка с помощью щекотки также полезна в некоторых случаях. Обычно производитель аккумуляторов предоставляет правильный метод зарядки определенных свинцово-кислотных аккумуляторов. Зарядка постоянным током обычно не используется при зарядке свинцово-кислотных аккумуляторов .
Наиболее распространенным методом зарядки, используемым в свинцово-кислотных аккумуляторах, является метод зарядки постоянным напряжением , который является эффективным с точки зрения времени зарядки.В полном цикле зарядки напряжение заряда остается постоянным, а ток постепенно уменьшается с увеличением уровня заряда аккумулятора.
Свинцово-кислотная батарея разряжаетсяРазрядка свинцово-кислотной батареи снова связана с химическими реакциями. Серная кислота находится в разбавленной форме, обычно в соотношении 3: 1 с водой и серной кислотой. Когда нагрузки подключаются поперек пластин, серная кислота снова распадается на положительные ионы 2H + и отрицательные ионы SO 4 .Ионы водорода реагируют с PbO 2 и образуют PbO и воду H 2 O. PbO начинает реагировать с H 2 SO 4 и создает PbSO 4 и H 2 O.
С другой стороны, ионы SO 4 — обмениваются электронами с Pb, образуя радикал SO 4 , который в дальнейшем создает PbSO 4 , реагирующий с Pb.
Как объяснено выше, следующие химические реакции происходят на аноде и катоде во время процесса разряда.Эти реакции прямо противоположны реакциям зарядки:
На катоде
Pb + SO 4 2- => PbSO 4 + 2e -
На аноде:
PbO 2 + SO 4 2- + 4H - + 2e - => PbSO 4 + 2H 2 O
В сочетании двух приведенных выше уравнений общая химическая реакция будет
.PbO 2 + Pb + 2H 2 SO 4 => 2PbSO 4 + 2H 2 O
Из-за обмена электронами между анодом и катодом нарушается баланс электронов на пластинах.Затем электроны проходят через нагрузку, и батарея разряжается.
Во время этого разряда плотность разбавленной серной кислоты уменьшается. Кроме того, в то же время уменьшается разность потенциалов ячейки.
Фактор риска и электрические характеристикиСвинцово-кислотный аккумулятор опасен при ненадлежащем обслуживании. Поскольку аккумулятор выделяет водород во время химического процесса, он очень опасен, если не используется в вентилируемом помещении.Кроме того, неточная зарядка серьезно повреждает аккумулятор.
Каковы стандартные характеристики свинцово-кислотных аккумуляторов?
Каждая свинцово-кислотная батарея снабжена таблицей данных по стандартному току заряда и току разряда. Обычно свинцово-кислотный аккумулятор на 12 В, применимый в автомобильной промышленности, может иметь диапазон от 100 Ач до 350 Ач. Этот рейтинг определяется как рейтинг разряда с 8-часовым периодом времени.
Например, батарея на 160 Ач может обеспечить 20 А питающего тока нагрузки в течение 8 часов диапазона .Мы можем потреблять больше тока, но делать это не рекомендуется. Потребление тока, превышающего максимальный ток разряда в течение 8 часов, приведет к снижению эффективности батареи, а также может измениться внутреннее сопротивление батареи, что еще больше увеличит температуру батареи.
С другой стороны, во время фазы зарядки, , мы должны быть осторожны с полярностью зарядного устройства , оно должно быть правильно подключено с полярностью батареи. Обратная полярность опасна для зарядки свинцово-кислотных аккумуляторов.Готовое зарядное устройство поставляется с измерителем зарядного напряжения и зарядного тока с возможностью управления. Мы должны обеспечить большее напряжение, чем напряжение батареи, чтобы зарядить батарею. Максимальный ток заряда должен быть таким же, как и максимальный ток питания при 8-часовой разряде. Если мы возьмем тот же пример 12 В 160 Ач, то максимальный ток питания составляет 20 А, поэтому максимальный безопасный ток зарядки составляет 20 А.
Не следует увеличивать или обеспечивать большой зарядный ток , так как это приведет к нагреву и увеличению газообразования.
Правила обслуживания свинцово-кислотных аккумуляторов- Полив — это функция, которой часто пренебрегают при обслуживании залитых свинцово-кислотных аккумуляторов. Поскольку перезарядка уменьшает воду, нам нужно часто ее проверять. Меньшее количество воды вызывает окисление пластин и сокращает срок службы батареи. При необходимости добавьте дистиллированную или ионизированную воду.
- Проверьте вентиляционные отверстия, их нужно усовершенствовать резиновыми заглушками, часто резиновые заглушки слишком плотно прилегают к отверстиям.
- Заряжайте свинцово-кислотные аккумуляторы после каждого использования. Длительный период без подзарядки обеспечивает сульфатирование в пластинах.
- Не замораживайте аккумулятор и не заряжайте его более чем на 49 градусов по Цельсию.


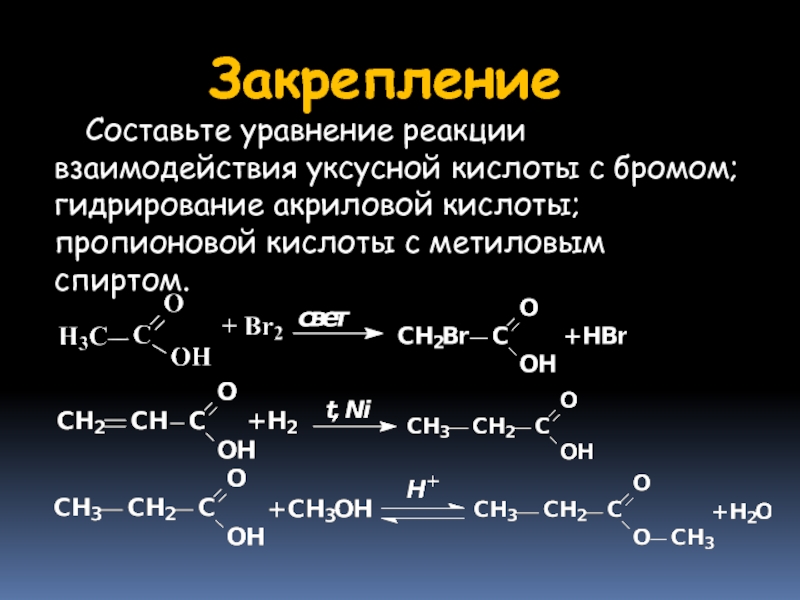
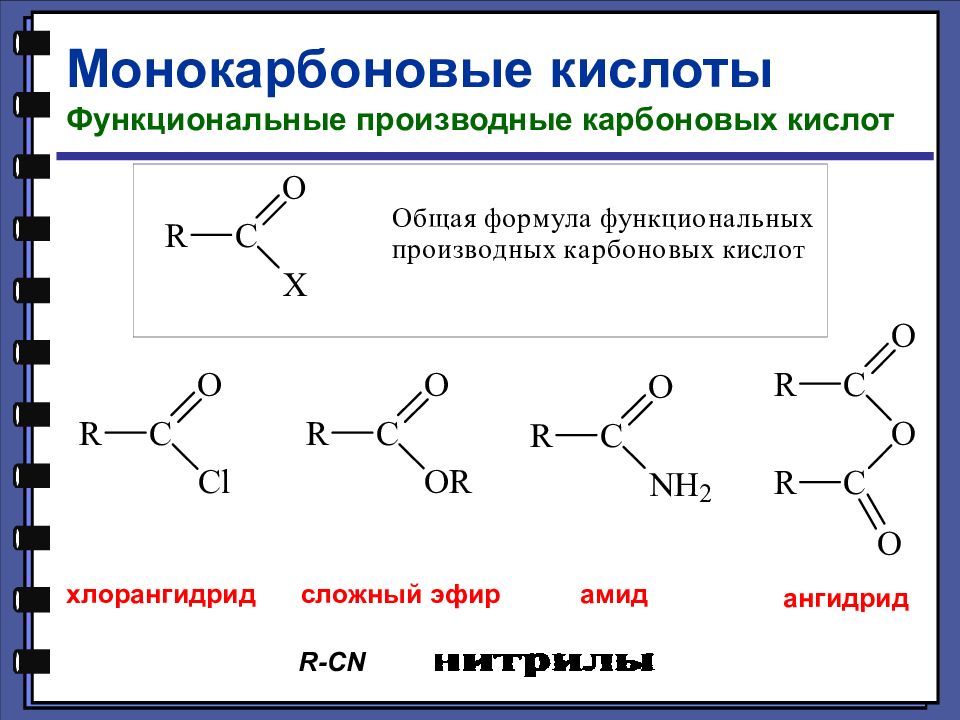 см;
см;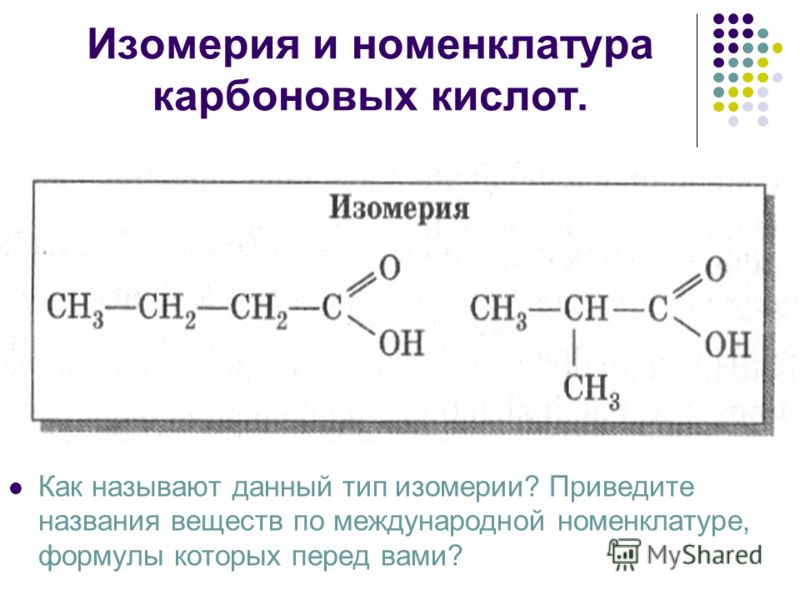
 Поэтому добавлять следует кислоты в дистиллированную воду тонкой струйкой.
Поэтому добавлять следует кислоты в дистиллированную воду тонкой струйкой.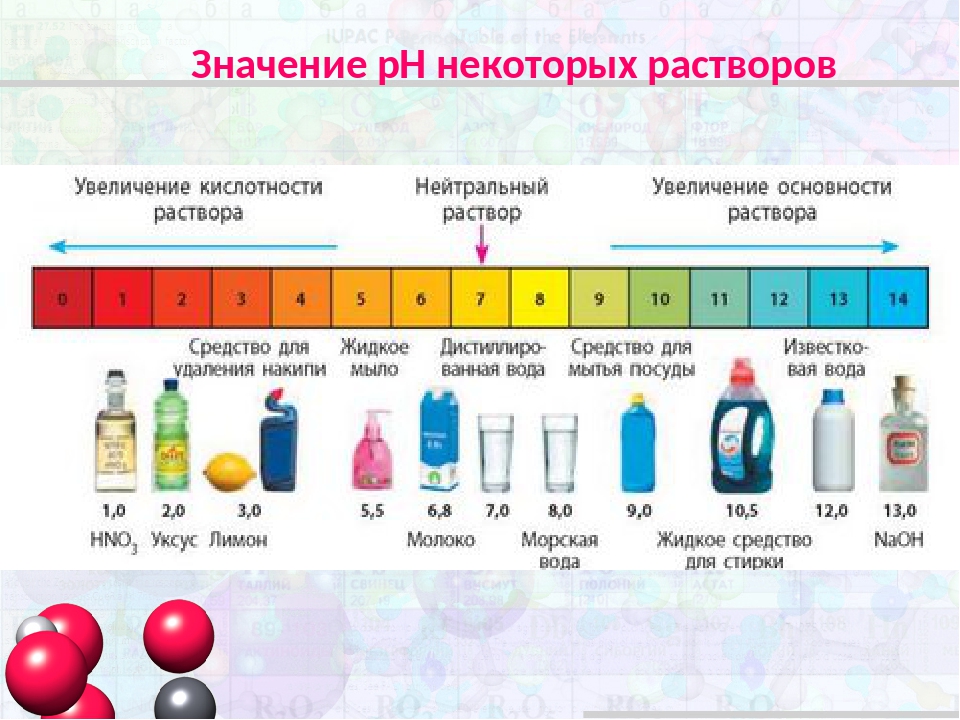
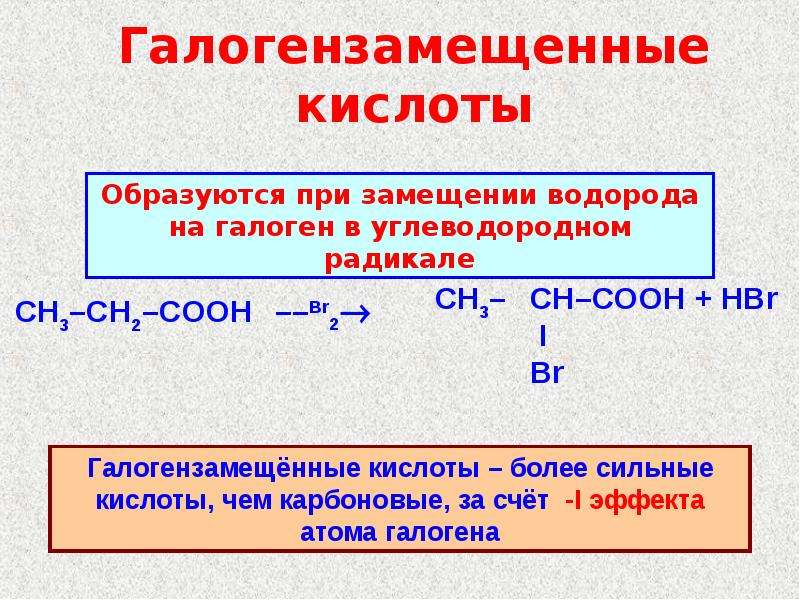 Этому пределу плотности соответствует концентрация h4SO4 27−40%.
Этому пределу плотности соответствует концентрация h4SO4 27−40%.