|
|
|
Освещая тему металлолома на нашем портале мы не могли обойти стороной автомобильные катализаторы. Ведь нередко в пункты приема металлолома поступают звонки с вопросами: «А вы катализаторы автомобильные покупаете?». Поэтому мы решили поделиться своими знаниями в этой области. Основным предназначением автокатализаторов в транспортных средствах является минимизация вредных выбросов в окружающую среду. В последнее время тема сохранения экологии актуальна как никогда. А вредные выбросы, являющиеся итогом отработки машинного топлива, содержат очень токсичные газы, которые наносят существенный ущерб как экологии нашей планеты, так и всем живым организмам. Поэтому применение катализаторов считается очень полезным. Из чего состоит и как устроено это техническое оборудование? Из чего состоит автомобильный катализатор Конвертор или автокатализатор имеет цилиндрическую форму с круглым или эллиптическим сечением, он изготовлен из керамики или металла, а также химических материалов с применением металлов платиновой группы. Насыщенность автокатализатора ценными элементами таблицы Менделеева открывает большие возможности для создания прибыльного дела на отработанных и пришедших в негодность автокатализаторах. Автокатализатор в разрезе Из школьного курса химии всем известно, что катализаторами являются определенные вещества, которые способны вызывать какую-либо химическую реакцию или ускорять процесс, при этом не входя в конечный продукт. Таким образом получается, что металлы платиновой группы никуда не исчезают, а наоборот, проявляются на керамической или металлической поверхности в виде тонюсенького платинового слоя. Именно они и проводят доокисление: Кроме всего сказанного, слой автокатализатора минимизирует образование частиц сажи, которые способствуют возникновению у человека онкологических заболеваний. Есть несколько способов получить драгоценные металлы из катализатора — это аффинаж и гидрохлорирование, а также способы электрохимической обработки. Аффинаж в утилизации катализаторов и добыче драгоценных металлов имеет такую же последовательность, как и при получения золота их микросхем. В емкость с концентрированной азотной кислотой помещаются части катализатора с содержанием платины — через несколько дней кислота растворит абсолютно всё, кроме драгоценных металлов. Аффинаж в данном случае не очень подходит для этого бизнеса, т.к.к нужны промышленные масштабы Гидрохлорирование, когда хлор воздействует на катализатор в диспергированном растворе или в водной среде, что также позволяет извлечь драгоценные металлы. Этот способ требует навыков и специального оборудования и больше подходит для промышленной добычи. Электрохимическая обработка — это травление, оксидирование и т.д. Этот способ позволяет избавиться от таких металлов, как хром, олово, свинец, цинк и алюминий. Также относится к промышленным способам утилизации автомобильных катализаторов. Сразу сделаем важное замечание, что утилизация автомобильных катализаторов и добыча из них драгоценных металлов — дело промышленников, т.к. чтобы при всех затратах на оборудование и материалы выйти «в плюс» нужно считать катализаторы тысячами, а то и десятками тысяч. Существуют специальные приборы для измерения содержания платиноидов методом рентгено-флюоресцентного анализа. Анализатор содержания металлов Сегодня в интернет-ресурсах достаточно часто можно встретить объявления о покупке пришедших в негодность автокатализаторов. Согласно последним данным статистик, в Европе спрос на б/у конверторы растет из года в год. И это неспроста. Такой бизнес очень быстро окупается. Как было сказано ранее, катализаторы, особенно те, которые установлены в современных европейских автомобилях, насыщены драгоценными металлами. К примеру, автомобили китайских и японских товаропроизводителей содержат на 15% меньше платины, чем европейские. А конверторы отечественных транспортных средств содержат на 40% меньше родия, чем европейские. В автокатализаторах американских автомобилей также на 50% меньше драгоценных металлов, чем в европейских. Для тех, кто забыл европейские марки авто, напомним — это BMW, Audi, Citroen, Volkswagen, Mersedes-Benz и другие. В последнее время спрос на платину значительно возрос, и он превышает предложение. Аффинаж драгоценных металлов из пришедших в негодность автокатализаторов становится все выгоднее. Эксперты многих стран считают, что если государство примет активное участие и сформирует определенные условия для этого вида бизнеса, он в ближайшем будущем выйдет на первые позиции в сфере ресурсосбережения. А создание приемлемого инвестиционного климата позволит ввести в действие разработку энергоемких технологий, которые будут ориентированы на самое результативное извлечение вторичного сырья. И когда этот бизнес станет расширяться, он позволит увеличить переработку конверторов, что повлечет за собой создание других предприятий и увеличение количества рабочих мест. Такие предприятия смогут также заниматься скупкой отработанных автокатализаторов у специализированных автосервисов и мастерских для последующей переработки. Здесь катализаторы будут вынуждены пройти весь необходимый цикл утилизации для последующего получения более полного списка драгоценных металлов. Да, для отечественных предпринимателей такой бизнес является чем-то новым, предстоит решить множество задач для его внедрения, но его эффективность и прибыльность давно доказана, поскольку количество транспортных средств будет постоянно увеличиваться, а рынок автокатализаторов будет расти и расширяться. И только поддержка подобного проекта государством обеспечит постепенное внедрение новейших отечественных технологий, которые будут способствовать стабилизации экосистемы в разных уголках нашей необъятной страны. Но надо реально смотреть на жизнь. Сегодня владельцы станций техобслуживания все чаще при обслуживании и замене автокатализаторов не упускают возможность получить прибыль и продают автолюбителям такие устройства. Стоит только набрать нужный номер фирмы и обсудить будущие условия сделки с руководством. xlom.ru Освещая тему металлолома на нашем портале мы не могли обойти стороной автомобильные катализаторы. Ведь нередко в пункты приема металлолома поступают звонки с вопросами: «А вы катализаторы автомобильные покупаете?». Поэтому мы решили поделиться своими знаниями в этой области. Основным предназначением автокатализаторов в транспортных средствах является минимизация вредных выбросов в окружающую среду. В последнее время тема сохранения экологии актуальна как никогда. А вредные выбросы, являющиеся итогом отработки машинного топлива, содержат очень токсичные газы, которые наносят существенный ущерб как экологии нашей планеты, так и всем живым организмам. Поэтому применение катализаторов считается очень полезным. Из чего состоит и как устроено это техническое оборудование? Из чего состоит автомобильный катализатор Конвертор или автокатализатор имеет цилиндрическую форму с круглым или эллиптическим сечением, он изготовлен из керамики или металла, а также химических материалов с применением металлов платиновой группы. Насыщенность автокатализатора ценными элементами таблицы Менделеева открывает большие возможности для создания прибыльного дела на отработанных и пришедших в негодность автокатализаторах. Автокатализатор в разрезе Из школьного курса химии всем известно, что катализаторами являются определенные вещества, которые способны вызывать какую-либо химическую реакцию или ускорять процесс, при этом не входя в конечный продукт. Таким образом получается, что металлы платиновой группы никуда не исчезают, а наоборот, проявляются на керамической или металлической поверхности в виде тонюсенького платинового слоя. Именно они и проводят доокисление: Кроме всего сказанного, слой автокатализатора минимизирует образование частиц сажи, которые способствуют возникновению у человека онкологических заболеваний. Есть несколько способов получить драгоценные металлы из катализатора — это аффинаж и гидрохлорирование, а также способы электрохимической обработки. Аффинаж в утилизации катализаторов и добыче драгоценных металлов имеет такую же последовательность, как и при получения золота их микросхем. В емкость с концентрированной азотной кислотой помещаются части катализатора с содержанием платины — через несколько дней кислота растворит абсолютно всё, кроме драгоценных металлов.Платиновый катализатор — сколько драгметалла содержится в детали автомобиля. Из чего сделан катализатор
Автомобильные катализаторы и бизнес
Немного теории

Как получают драгоценные металлы?


Каковы реальные перспективы развития бизнеса на б/у катализаторах?
Как дело обстоит в России?
Способ извлечения платиновых металлов из автомобильных катализаторов. Из чего сделан катализатор
Автомобильные катализаторы и бизнес
Немного теории


Как получают драгоценные металлы?

auto21rus.ru
сколько содержится чистого драгметалла в детали автомобиля, как извлечь платину своими руками

Платиновый катализатор сегодня используется во многих автомобилях. Он является одним из основных элементов выхлопной системы и обеспечивает снижение уровня вредных выбросов. Его корпус покрыт драгоценными металлами, которые, при наличии определенных условий, можно извлечь. Однако сложно заранее предугадать, сколько платины содержится в катализаторе автомобиля.
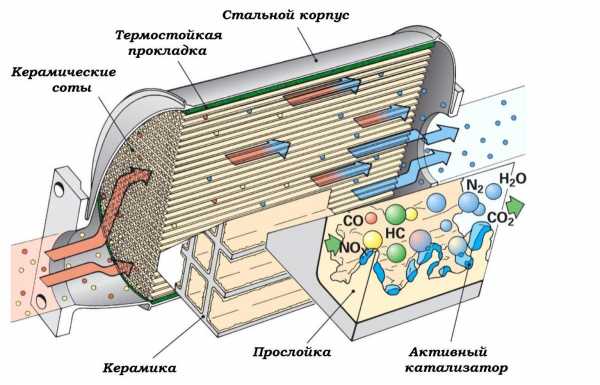
Конструкция катализатора
Внутренняя часть автомобильного компонента заполнена особой конструкцией, выполненной из керамики или металла. Внешне она напоминает пчелиные соты. Верхняя часть катализатора покрыта тонким слоем драгоценного металла.
Наличие такого напыления обеспечивает снижение уровня вредных выбросов. Это достигается за счет того, что выхлопные газы, контактируя с драгметаллами и другими веществами, вступают с ними в химическую реакцию. Для напыления внутренней части автокомпонента используют сочетание:
- платины;
- родия;
- палладия.
Каждый из этих металлов оценивается довольно высоко. Поэтому автомобильные катализаторы привлекают многих людей, которые занимаются извлечением драгоценных материалов с целью их дальнейшей перепродажи.
Добычи указанных металлов – это довольно сложный процесс, требующий наличия соответствующих навыков и различных дорогостоящих веществ.
Существует несколько технологий, посредством которых можно извлекать драгметаллы. Они подбираются исходя из конечных целей работы.

Некоторые из указанных технологий, а также их результаты приведены в таблице.
| Выщелачивание посредством окислителей | Платина и родий |
| Гальванический метод | Палладий |
| Воздействие «Царской водкой» | Платина |
| Фторирование | Палладий |
Выбор в пользу конкретной технологии обусловлен в основном возможностями человека, который получает платину из катализатора. Также важно понимать, что в процессе аффинажа существуют неизбежные потери извлекаемых материалов. В частности, подобные недостатки отмечаются у техники выщелачивания, которая требует многократных промывок компонентов химической реакции.
Поверхность автокатализаторов покрыта напылением драгоценных металлов. Эти материалы, при наличии соответствующих навыков и реагентов, можно извлечь.
Техника выщелачивания
В домашних условиях и в промышленности для выделения родия и палладия чаще применяют выщелачивания. Такая техника предполагает использование окисляющих растворов, состоящих из концентрированных соляной и азотной кислот. При этом выщелачивание имеет ряд существенных недостатков отчасти обусловленных особенностями конструкции автомобильного катализатора.
Последний изготавливается либо из керамики, либо из алюминия. Наличие этого металла затрудняет проведение аффинажа, так как окислители вступают с ним реакцию. В процессе выделения платины, которая извлекается в виде раствора, необходимо многократное повторение выщелачивания и промывки исходных компонентов. Более того, даже такой подход не позволяет добыть драгоценный металл в достаточном количестве: избежать потери невозможно. Соответственно, для извлечения платины потребуется несколько катализаторов.
В целях снижения потерь, возникающих во время проведения аффинажа, автокомпонент на начальном этапе смачивают в водном растворе соляной кислоты. В дальнейшем катализатор подвергается нагреву. Далее, когда под воздействием высокой температуры появились пары, на исходный компонент наносятся окислители.

Кроме того, в зависимости от состава сплава, который напылялся на поверхность катализатора, для проведения аффинажа можно применить смесь концентрированной азотной кислоты и 30-процентного раствора пероксида водорода.
В промышленных масштабах для извлечения платины используют специальную решетчатую сетку, на которую помещается деталь. На нее затем оказывают воздействие парообразного окислителя. Для этого сначала заготавливают раствор соляной кислоты, в которую помещается деталь, а затем ее доводят до кипения. По окончании этого процесса, в ходе которого пары многократно проходят через каналы и поры катализатора, последний подвергается промывке чистой водой.
Использование парообразного окислителя имеет несколько преимуществ в сравнении с жидкостными кислотами. Основное отличие между двумя приведенными выше подходами заключается в том, что газовая смесь обладает большей проникающей способностью. Поэтому она лучше «промывает» катализатор, затрагивая даже мелкодисперсные частицы.
Особенности добычи палладия
Для извлечения палладия из автомобильного катализатора можно применять техники, описанные выше. Но в таком случае полученный металл включает в себя множество примесей, что снижает его ценность. Наиболее действенным способом добычи палладия из автомобильных деталей считается электродуговое нагревание (гальванический метод).
Однако предпочтительнее использовать несколько иной подход. Он предполагает нагревание исходного компонента до 500 градусов с последующим фторированием. Эта технология позволяет получить металл с минимальным содержанием разнообразных примесей. Результатом данного процесса становится фтористый палладий, который необходимо остудить до 100 градусов. Для выделения чистого металла из раствора потребуется минеральная кислота.
Метод фторирования позволяет выделить практически весь палладий, что содержит в себе автомобильный катализатор.
Примеры выделения драгоценных металлов
Ниже приведены три примера, наглядно объясняющие процесс выделения драгоценных металлов из автомобильных компонентов.
Пример 1.В данном примере используется катализатор с автомобиля марки Volvo. Его сплав состоит из палладия (0,08% от общей массы компонентов) и родия (0,006%). Ввиду того что в исходной детали содержится углерод в относительно большом количестве, ее предварительно обжигают, в течение 45 минут оказывая воздействие при температуре в 540 градусов. Далее смешиваются между собой 230 мл воды и 46 мл концентрированной соляной кислоты. После этого в раствор добавляются 184 мл пироксида углерода, после чего его нагревают. Аффинаж проводится на протяжении 1 часа.
Пример 2.Для извлечения драгметаллов используется 1,2-киллорамовый катализатор, взятый с автомобиля марки Mercedes-Benz. В составе его сплава встречаются платина (0,12% от общей массы детали) и родий (0,008%).

Автокомпонент помещается во фторопластовый реактор. Далее он смачивается посредством 260 мл водного раствора соляной кислоты. После этого автокомпонет подвергается воздействию 70 мл данной кислоты, используемой в чистом виде.
Далее раствор доводится до кипения. В процессе нагрева в смесь добавляются 60 мл концентрированной азотной кислоты и 150 мл 30-процентного раствора пероксида водорода. Этот элемент вводится по частям. Аффинаж палладия занимает около 1,5 часа. По истечении указанного срока полученный раствор промывается водой (1 к 2) и осаждается.
Пример 3.В последнем примере применяется катализатор от автомобиля Honda. В составе сплава встречаются платина (0,04% от общего веса детали), палладий (0,06%), родий (0,007%) и церий (1,4%). Подход в данном случае используется тот же, что был приведен в предыдущем примере. Разница между техниками добычи наблюдается только на конечном этапе. Достигнув точки кипения, автокомпонент обрабатывается соляно-азотной кислотой и пероксидом водорода.
Применение выщелачивания позволяет получить из автокатализаторов относительно чистые драгоценные металлы, пригодные для повторного использования.
prodragmetally.ru
Катализатор - это... Что такое Катализатор?
 Схема протекания реакции с катализатором
Схема протекания реакции с катализатором Катализа́тор — химическое вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции[1]. Количество катализатора, в отличие от реагентов, после реакции не изменяется. Важно понимать, что катализатор не участвует в реакции. Они обеспечивают более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. Затем катализатор снова реагирует с исходным веществом, и этот каталитический цикл многократно повторяется.
Катализаторы в химии
Катализаторы подразделяются на гомогенные и гетерогенные. Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный — образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества [1]. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al2O3, TiO2, ThO2, алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO [1].
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных, существуют катализаторы окисления-восстановления; для них характерно присутствие переходного металла или его соединения (Со+3, V2O5+MoO3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Много реакций осуществлено при помощи катализаторов, которые действуют через координацию реагентов у атома или иона переходного металла (Ti, Rh, Ni). Такой катализ называется координационным.
Если катализатор обладает хиральными свойствами, то из оптически неактивного субстрата получается оптически активный продукт.
В современной науке и технике часто применяют системы из нескольких катализаторов, каждый из которых ускоряет разные стадии реакции [2][3]. Катализатор также может увеличивать скорость одной из стадий каталитического цикла, осуществляемого другим катализатором. Здесь имеет место «катализ катализа», или катализ второго уровня (Имянитов).
В биохимических реакциях роль катализаторов играют ферменты.
Катализаторы следует отличать от инициаторов. Например, перекиси распадаются на свободные радикалы, которые могут инициировать радикальные цепные реакции. Инициаторы расходуются в процессе реакции, поэтому их нельзя считать катализаторами.
Ингибиторы иногда ошибочно считают отрицательными катализаторами. Но ингибиторы, например, цепных радикальных реакций, реагируют со свободными радикалами и, в отличие от катализаторов, не сохраняются. Другие ингибиторы (каталитические яды) связываются с катализатором и его дезактивируют, здесь имеет место подавление катализа, а не отрицательный катализ. Отрицательный катализ в принципе невозможен: он обеспечивал бы для реакции более медленный путь, но реакция, естественно, пойдёт по более быстрому, в данном случае, не катализированному, пути.
Катализаторы в автомобилях
Задачей автомобильного катализатора является снижение количества вредных веществ в выхлопных газах. Среди них:
- окись углерода (СО) — ядовитый газ без цвета и запаха
- углеводороды, также известные как летучие органические соединения — один из главных компонентов смога, образуется за счёт неполного сгорания топлива
- оксиды азота (NO и NO2, которые часто объединяют под обозначением NOx) — также являются компонентом смога, а также кислотных дождей, оказывают влияние на слизистую человека.[4]
Источники
- ↑ 1 2 3 Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — Т. 2. — С. 335, 337. — ISBN 5-85270-035-5.
- ↑ Имянитов Н. С. Системы из нескольких катализаторов в металлокомплексном катализе. // Координационная химия. 1984. — Т. 10. — № 11 — С. 1443—1454. — ISSN 0132-344X.
- ↑ Temkin O.N., Braylovskiy S. M. / The mechanism of catalysis in homogeneous polyfunctional catalytic systems. // Fundamental Research in Homogeneous Catalysis. — Ed. by A.E. Shilov. — New York etc: Gordon and Breach Science Publishers, 1986. — Vol. Two. — P.621- 633.
- ↑ Автомобильный катализатор и его роль в выхлопной системе. AutoRelease.ru. Архивировано из первоисточника 25 августа 2011.
См. также
Ссылки
dic.academic.ru
Способ извлечения платиновых металлов из автомобильных катализаторов
Предложен способ извлечения суммы благородных металлов из скрапа отработанных автокатализаторов. Он предусматривает перевод платиновых металлов в водорастворимое состояние путем предварительного смачивания катализатора соляной кислотой с дальнейшим окислительным растворением, осуществляемым известными окислителями, например азотной кислотой или раствором пероксида водорода. Процесс ведут при нагреве для многократной циркуляции парогазовой выщелачивающей смеси. Способ достаточно прост и позволяет вовлекать в переработку катализаторы с различным сочетанием платиновых металлов при низких реагентных затратах со снижением потерь извлекаемых металлов. 2 з. п. ф-лы.
Изобретение относится к области металлургии платиновых металлов, использующей в качестве исходного вторичное техногенное сырье, а именно скрап отработанных автомобильных катализаторов, где платиноиды применяются в виде двойных или тройных систем, например Pt/Rh, Pd/Rh, Pt/Pd/Rh, нанесенных на сотообразные блоки, изготовленные из кордиерита.
Известны способы извлечения каталитических компонентов металлов платиновой группы путем их окисления газообразными реагентами (окислительный обжиг с кислородом, хлорирование, фторирование) [патент Японии 54-14571 от 08.06.79, Патент США 4069040 от 17.01.78, патент США 4077800 от 07.03.78, заявитель ЧССР, Precious Metals 89. Proc. Int. Symp. TMS Annu. Meet., Las Vegas, 483-501] с последующим их отделением от основы. В данных случаях, например хлорировании, проводят высокотемпературную обработку до образования летучих карбонилхлоридов платины, которые улавливают абсорбцией и выделяют металл восстановительным осаждением. Рассматривая подробно сведения о режимах проведения данных процессов с применением газообразных окислителей, справедливо отметить, что они не вполне пригодны для переработки катализаторов-дожигателей моторных топлив. Высокоагрессивные газообразные реагенты весьма опасны в работе и требуют использования дорогостоящего оборудования, соблюдения повышенных мер безопасности, необходимости строгой утилизации ядовитых соединений. Широко представлены способы извлечения драгметаллов путем их окисления и выщелачивания жидкими растворителями, например царской водкой, азотной кислотой, смесью соляной кислоты и пероксида водорода, растворами хлора в кислотах, гипохлоритами [Precious and Rare Metal Technol., Proc Symp. Precious and Rare Metals Albuguergue, N. M., Apr. 6-8, 1988./Amsterdam etc., 1989. -P.345-363, Precious Metals 89. Proc. Int. Svmp. IMS Annu, Meet., Las Vegas, Nev, Febr. 27 - March 2, 1989. - Warrendale (Pa), 1989. - p. 483-501, патент 1228989. Канада, С 22 В 11/06, заяв. 5.10.84, от 10.11.87]. Анализ этих патентных публикаций приводит к выводу об их ориентации на определенный тип сырья при достаточно низкой степени извлечения ценных компонентов. При этом, как правило, данные процессы характеризуются сложным аппаратурно-технологическим оформлением, многостадийны и энергоемки. Наиболее близким к заявляемому является способ выщелачивания благородных металлов жидкими окисляющими растворами или смесями, например царской водкой [Тематический обзор. Извлечение ценных металлов из отработанных гетерогенных катализаторов. ЦНИИТЭнефтехим, М., 1988, с. 29]. Несмотря на дешевизну применяемых кислот и освоенность работы с царской водкой на аффинажных производствах, включая последующую газоочистку, данный способ не лишен существенных недостатков при использовании его для переработки автокатализаторов. Наличие в блоках сотовых катализаторов-нейтрализаторов выхлопа двигателей подслоя из активной окиси алюминия, на который наносятся каталитические элементы, определяет трудность полного снятия этих благородных металлов. При жидкофазном выщелачивании из-за высокой величины поверхности у гамма-окиси алюминия (до 200 м2/г) всегда происходят два конкурентных процесса: десорбция соединений платиновых металлов в раствор с поверхности катализатора и обратная сорбция на нее. Именно это обратимое равновесие для своего смещения требует многократных процедур выщелачивания и промывки, которые в итоге не всегда обеспечивают полноту снятия металлов. Последнее обстоятельство также приводит к неизбежным реагентным и энергетическим затратам из-за необходимости переработки больших объемов с низкой концентрацией ценных компонентов. Эти недостатки, в конечном итоге, определяют высокие необратимые потери извлекаемых металлов. Главной задачей настоящего изобретения, решение которой приводит к получению технического результата, является проведение процесса выщелачивания таким образом, чтобы постоянно изменять концентрацию окисленных металлов в сторону раствора для снижения потерь извлекаемых металлов. Технический результат достигается способом извлечения платиновых металлов из автомобильных катализаторов, включающим растворение кислотно-окисляющей смесью, согласно изобретению перед растворением проводят смачивание катализатора водным раствором соляной кислоты в соотношении НСl:Н2O=1: 1-5, растворение ведут последующим нагревом с добавлением окислителей при кипении в парах окисляющих реагентов, и после промывки осадка водой из полученных растворов осаждают металлы цементацией в коллективный концентрат. Кроме этого, растворение осуществляют в зависимости от состава сырья с использованием в качестве окислителя концентрированной азотной кислоты и(или) 30%-го раствора пероксида водорода, а также растворение проводят в замкнутом цикле при испарении и конденсации. Известные кислотные смеси, окисляющие платиновые металлы, используют как в виде жидкости, так и в виде пара. Именно перевод в газообразное состояние снимает диффузионные затруднения контакта реагентов с каталитическими металлами и обеспечивает полноту их перевода в раствор. Для этого катализаторные блоки загружают в реактор на специальную решетчатую полку, орошают предварительно приготовленным раствором соляной кислоты, выполняющим роль и комплексообразователя и пропиточного раствора. Его объем регулируется таким образом, чтобы катализатор при этом всегда располагался выше уровня жидкости. Затем включается электрическая схема нагрева реактора и реакционную жидкость доводят до кипения. Процесс ведется в течение определенного времени, за которое происходит многократная циркуляция паров окислителя в каналах и порах катализатора и последующий слив по ним конденсата. При этом роль конденсора на себя берут сами блоки до тех пор, пока не будет достигнуто тепловое равновесие. По завершении этой стадии полученный раствор направляется на фильтрацию, а катализатор промывают водой и промводы объединяют с основным раствором. Выделение платиновых металлов и присутствующего в рецептурном составе редкоземельного церия из полученного раствора ведут известными способами. Таким образом, главным отличительным признаком заявляемого способа является применение стандартных окисляющих смесей, учитывающих химическую активность конкретного металла, входящего в состав катализатора в парообразном и жидком состояниях. Это позволяет не только увеличить проникающую способность газовой смеси, но и осуществить многократное омывание мелкодисперсных частиц платиновых металлов всегда "свежим" раствором. Другое отличие заключается в возможности строгой дозировки окислителя, например, азотной кислоты и применения "обедненной" по НNО3 царской водки, достаточной лишь на растворение целевых металлов и других примесей, образовавшихся в период эксплуатации блока. Реализация этих признаков становится возможным из-за работы по принципу замкнутого цикла: испарение-конденсация-смыв. Технический результат изобретения достигается еще и специальной конструкцией реактора получения основного раствора, который представляет собой модифицированную колонну, где роль флегмовых тарелочек выполняют каналы блоков катализатора. Отчасти по своей сути, он напоминает модифицированный к конкретным условиям задачи аппарат Сокслета, применяемый в органической химии для экстракции из твердых веществ ценных компонентов легколетучими растворителями. Таким образом, главным следствием, определяющим существо предлагаемого способа, является высокая степень извлечения в раствор металлов платиновой группы, получение их растворов с высокой концентрацией, малый расход реагентов по сравнению с другими способами-аналогами. Заявляемый способ является общим, поскольку позволяет не только вовлекать в переработку блочные катализаторы с любой комбинацией благородных металлов, но и попутно выделять церий, входящий в состав этих композиций для уменьшения коэффициента термического расширения. Расчетно дозируемое количество высокоагрессивных окислителей резко снижает нагрузку на очистные устройства и позволяет успешно решить экологические проблемы производства как в виде газовых выбросов, так и сливных растворов. Пример 1 Отработанный катализатор с автомобиля "Mercedes-Benz" массой 1,2 кг имеет в качестве каталитических металлов платину и родий, остаточное содержание которых 0,12 и 0,008 мас.% соответственно. Ввиду малого количества углерода, не превышающего 2,2 мас.%, предварительной подготовки путем обжига не проводится. Катализатор помещают в реактор из фторопласта, смачивают водным раствором НСl (1:1) в количестве 260 мл (25% от исходной массы катализатора). Затем в реактор добавляют остаток НСl в количестве 70 мл. Реакционную смесь нагревают до кипения и последовательно вводят 60 мл концентрированной НNO3 и по частям 150 мл 30%-ного раствора пероксида водорода. Процесс выщелачивания продолжают в течение 1,5 ч. Затем нагрев снимают и катализатор промывают дистиллированной водой в соотношении ж:т, как 2:1. Из основного раствора, объединенного с промводами, осаждают коллективный платино-родиевый концентрат цементацией алюминиевым порошком. Сквозное извлечение металлов в концентрат составляет 98,6% по платине и 94,8% по родию. Пример 2 Палладий-родиевый катализатор автомобиля "Volvo" по данным химического анализа содержит 0,08 мас.% палладия и 0,006 мас.% родия. Кроме этого, на катализаторе присутствуют значительные отложения пироуглерода, массовая доля которого составляет 8,7 мас.%. Из-за высокого содержания сажи до проведения процесса переработки катализатор подвергается предварительному обжигу при температуре 540oС в течение 45 мин. Последующая пропитка охлажденного катализатора проводится раствором от смешения 46 мл НСl конц. и 230 мл Н2O. После внесения 184 мл 30%-ного раствора Н2О2, реакционная смесь общим количеством 460 мл ставится на нагрев. Температурную обработку после начала кипения проводят в течение 1 ч. Выход аффинированных металлов чистотой 99,5% составляет для палладия 97,8% (0,8810) г и для родия 92,4% (0,0624) г. Пример 3 Дезактивированный катализатор автомобиля "Honda" имеет в своем составе 0,04% платины, 0,06% палладия, 0,007% родия и 1,4% церия. Катализатор заливают на холоду 250 мл водного раствора НСl (1:1). После достижения температуры кипения проводится последовательная обработка раствором царской водки с последующим введением пероксида водорода по условиям примера 1. В результате дальнейшей переработки суммарное извлечение аффинированных металлов к исходному содержанию составляет - платины 0,3878 г (98,0%), палладия 0,5831 г (98,2%) и родия 0,0653 г (94,1%). Таким образом лабораторные и полупромышленные испытания технологической цепочки переработки катализаторов-нейтрализаторов выхлопа моторных топлив от их выщелачивания до получения товарных металлических черней платиновых металлов позволяет значительно сократить расходы на реагенты и уменьшить затраты на газоочистку. Кроме этого, представляется возможным повторно использовать кордиерит - ценный материал носителя катализатора для изготовления новых блоков-дожигателей.Формула изобретения
1. Способ извлечения платиновых металлов из автомобильных катализаторов, включающий растворение кислотно-окисляющей смесью, отличающийся тем, что перед растворением проводят смачивание катализатора водным раствором соляной кислоты в соотношении HCl:Н2О=1:1-5, растворение ведут последующим нагревом с добавлением окислителей при кипении в парах окисляющих реагентов, и после промывки осадка водой из полученных растворов осаждают металлы цементацией в коллективный концентрат. 2. Способ по п.1, отличающийся тем, что растворение осуществляют в зависимости от состава сырья с использованием в качестве окислителя концентрированной азотной кислоты и/или 30%-ного раствора пероксида водорода. 3. Способ по п.1, отличающийся тем, что растворение проводят в замкнутом цикле при испарении и конденсации.www.findpatent.ru
Катализатор | Химическая энциклопедия
Одно из наиболее эффективных воздействий на химические реакции – это применение катализатора. Катализаторы – это вещества, ускоряющие химические реакции. Присутствие катализаторов изменяет скорость реакции в тысячи и даже миллионы раз. Катализаторы активно участвуют в химической реакции, но в отличие от реагентов в конце ее остаются неизменными.
Катализаторы – это вещества, которые изменяют скорость протекания реакции, но сами не расходуются в ходе реакции и не входят в состав конечных продуктов.
Важной характеристикой каталитической реакции (катализа) является однородность или неоднородность катализатора и реагирующих веществ. Различают гомогенные и гетерогенные каталитические процессы. При гомогенном (однородном) катализе между реагирующими веществами и катализатором отсутствует поверхность раздела. В данном случае катализ осуществляется через образование неустойчивых промежуточных продуктов.
Например, вещество A должно вступить в реакцию с веществом B. Однако для начала реакции необходимо сильное нагревание, и реакция далее протекает медленно. Тогда подбирают катализатор с таким расчетом, чтобы он с веществом A образовал активное промежуточное соединение, способное потом энергично реагировать с веществом B:
A + Кат. = A ∙ Кат. A ∙ Кат. + B = AB ∙ Кат. Кат. A + B = AB
Процессы, в которых катализатор и катализируемые вещества находятся в разных агрегатных состояниях, относятся к гетерогенному (неоднородному) катализу. При адсорбции на поверхности катализатора газообразных или жидких реагентов ослабляются химические связи, возрастает способность этих веществ к взаимодействию.
Ускоряющее действие катализатора заключается в понижении энергии активации основной реакции. Каждый из промежуточных процессов с участием катализатора протекает с меньшей энергией активации, чем некатализируемая реакция. Катализ открывает иной пут протекания химической реакции от исходных веществ к продуктам реакции.
Опыт показывает, что катализаторы строго специфичны для конкретных реакций. Например, в реакции:
N2+3h3 =Fe 2Nh4
Катализатором является металлическое железо, а в реакции окисления оксида серы(IV) в оксид серы(VI) катализатор – оксид ванадия(V) V2O5. Часто в качестве катализаторов используют платину, никель, палладий, оксид алюминия. Для ускорения процесса разложения пероксида водорода в качестве катализатора применяют оксид марганца(IV). Если в стакан с раствором пероксида водорода добавить немного оксида марганца(IV), сразу происходит бурное вспенивание жидкости в результате выделения кислорода.
Катализатором реакции взаимодействия алюминия и йода является обычная вода. Если к смеси алюминия и йода прилить воду, то вещества в смеси бурно реагируют.
Существуют вещества, способные замедлять химическую реакцию – осуществлять так называемый отрицательный катализ. Их называют ингибиторами. Такие вещества применяют при необходимости замедлит некоторые процессы, например коррозию металлов, окисление сульфидов при хранении и др. Вам необходимо включить JavaScript, чтобы проголосовать
abouthist.net

 Добавить сайт в избранное
Добавить сайт в избранное















.jpg)

